Teoria do mar dos fundamentos e propriedades de elétrons
- 2391
- 216
- Pete Wuckert
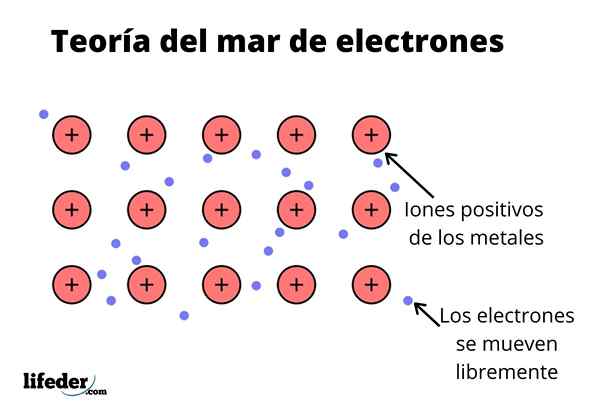
O Teoria do Sea Eletrônico É uma hipótese que explica um fenômeno químico excepcional que ocorre em ligações metálicas entre elementos com baixas eletronegatividades. Este é o compartilhamento de elétrons entre diferentes átomos unidos através de ligações metálicas.
A densidade eletrônica entre essas ligações é tal que os elétrons são realocados e formam um "mar" onde se movem livremente. Também pode ser expresso pela mecânica quântica: alguns elétrons (geralmente existem um a sete por átomo) são dispostos em orbitais com vários centros que são esticados pela superfície metálica.
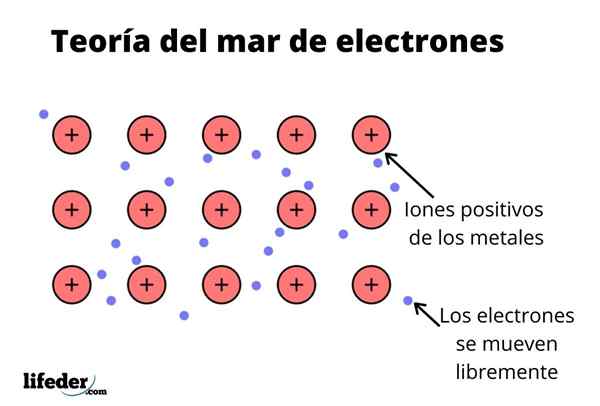
Além disso, os elétrons mantêm algum local em metal, embora a distribuição de probabilidade da nuvem eletrônica tenha maior densidade em torno de alguns átomos específicos. Isso ocorre porque quando uma corrente específica é aplicada, eles manifestam sua condutividade em uma direção específica.
[TOC]
Fundamentos da teoria do mar eletrônico
Os elementos metálicos têm uma grande tendência a doar elétrons de seu mais recente nível de energia (camada de valência), devido à sua baixa energia de ionização em relação aos outros elementos.
Sabendo disso, cada elemento metálico pode ser considerado como um cátion ligado ao elétron de seu último nível de energia, o que seria mais propenso a doar.
Como em um metal, há um grande número de átomos que estão ligados entre si, pode -se supor que esse metal forma um grupo de cátions metálicos que são mergulhados em uma espécie de mar de elétrons de valência que têm grande realocação.
Considerando que as forças de atração eletrostática entre o cátion (carga positiva) e o elétron (carga negativa) têm os átomos do metal fortemente ligados, imagine a realocação dos elétrons de valência se comportando como um adesivo eletrostático que retém ligados a cátions metálicos.
Pode atendê -lo: polímerosDessa maneira, pode -se inferir que quanto maior o número de elétrons presentes na camada de Valência de um metal, esse tipo de adesivo eletrostático terá uma força maior.
Propriedades
A teoria do mar eletrônico oferece uma explicação simples para as características de espécies metálicas, como resistência, condutividade, ductilidade e maleabilidade, que variam de um metal para outro.
Foi descoberto que a resistência conferida aos metais se deve à grande realocação de seus elétrons, o que gera uma força de coesão muito alta entre os átomos que o formam.
Dessa maneira, a ductilidade é conhecida como a capacidade de certos materiais de permitir a deformação de sua estrutura, sem dar o suficiente para quebrar, quando são submetidos a certas forças.
Delocalização na forma de camadas
Tanto a ductilidade quanto a maleabilidade de um metal são determinadas pelo fato de que os elétrons de Valência são democados em todas as direções na forma de camadas, o que os faz se deslocar antes da ação de uma força externa, evitando a quebra da estrutura metálica, mas permitir sua deformação.
Da mesma forma, a liberdade de movimento de elétrons realocados permite que um fluxo de corrente elétrica seja, fazendo com que os metais tenham muito boa condutividade de eletricidade.
Além disso, esse fenômeno de livre circulação de elétrons permite a transferência de energia cinética entre as diferentes regiões metálicas, o que promove a transmissão de calor e faz com que os metais manifestem uma grande condutividade térmica.
Pode atendê -lo: Iodose ácido (hio2): propriedades e usosTeoria do mar de elétrons em cristais de metal
Os cristais são substâncias sólidas que têm propriedades físicas e químicas - como densidade, fusão e dureza - que são estabelecidos pelo tipo de forças que fazem as partículas que compõem -as são mantidas juntas.
De certa forma, considera -se que os cristais metálicos têm as estruturas mais simples, porque cada "ponto" da rede de vidro foi ocupado por um átomo do próprio metal.
Nesse mesmo sentido, foi determinado que a estrutura dos cristais de metal é geralmente cúbica e se concentra em rostos ou corpo.
No entanto, essas espécies também podem ter uma forma hexagonal e ter uma embalagem bastante compacta, o que lhes dá aquela densidade enorme que é característica deles.
Devido a esse motivo estrutural, os links formados em cristais de metal são diferentes daqueles que ocorrem em outras classes de cristais. Em toda a estrutura cristalina, elétrons que podem formar ligações, conforme explicado acima, são explicados anteriormente.

Desvantagens da teoria
Nos átomos de metal, há uma pequena quantidade de elétrons de valência proporcional aos seus níveis de energia; Ou seja, há uma quantidade maior de estados de energia disponíveis do que a quantidade de elétrons vinculados.
Isso implica que, como existe uma forte realocação eletrônica e também bandas de energia que preenchem parcialmente, os elétrons podem se mover pela estrutura reticular quando são submetidos a um campo elétrico do exterior, além de formar o oceano eletrônico que admite a permeabilidade de a rede.
Pode servir você: oxácidoPortanto, a união dos metais é interpretada como um conglomerado de íons positivos acoplados por um mar de elétrons (carga negativa).
No entanto, existem características que não são explicadas através desse modelo, como a formação de certas ligas entre metais com composições específicas ou a estabilidade de links de metal coletivo, entre outros.
Esses inconvenientes são explicados pela mecânica quântica, porque tanto essa teoria quanto muitas outras abordagens foram estabelecidas com base no modelo mais simples de um único elétron, enquanto tentam se aplicar em estruturas muito mais complexas de átomos multieletrônicos.
Referências
- Wikipedia. (2018). Wikipedia. Recuperado de.Wikipedia.org
- Holman, j. S., E Stone, P. (2001). Química. Recuperado de livros.Google.co.ir
- Parkin, g. (2010). Ligação metal-metal. Recuperado de livros.Google.co.ir
- Rohrer, g. S. (2001). Estrutura e ligação em materiais cristalinos. Recuperado de livros.Google.co.ir
- Ibach, h., e Lüth, H. (2009). Física de Estado Sólido: Uma Introdução aos Princípios da Ciência dos Materiais. Recuperado de livros.Google.co.ir
- « Processo de hibridação cultural, tipos e exemplos
- 20 Locais turísticos de Aguascalientes (fotos) »

