Sulfeto de zinco (ZnS)
- 4319
- 908
- Conrad Schmidt
 Sulfeto de zinco. Fonte: Wikimedia Commons
Sulfeto de zinco. Fonte: Wikimedia Commons O que é sulfeto de zinco?
Ele Sulfeto de zinco É um composto inorgânico da Fórmula ZnS, formado por cátions Zn2+ e ânions s2-. É encontrado na natureza principalmente como dois minerais: o Wurtzite e o Spheny (ou Blenda de Zinco), sendo este último a sua principal forma.
O Sphenhell é apresentado na natureza negra devido às impurezas que apresenta. Puramente apresenta cristais brancos, enquanto o Wurtzita tem cristais brancos acinzentados.
O sulfeto de zinco é insolúvel em água. Pode causar danos ambientais, pois penetra no solo e contamina as águas subterrâneas e suas correntes.
O sulfeto de zinco pode ocorrer, entre outras reações, corrosão e neutralização.
Por corrosão:
Zn +h2S => ZnS +H2
Por neutralização:
H2S +Zn (OH)2 => ZnS +2h2QUALQUER
O sulfeto de zinco é um sal fosforescente, o que lhe dá a capacidade de múltiplos usos e aplicações. Além disso, é um semicondutor e um fotocatizante.
Estrutura do sulfeto de zinco
O sulfeto de zinco adota estruturas cristalinas governadas por atrações eletrostáticas entre o Zn Cation2+ e ânion s2-. Estes são dois: o Spheny ou o zinco Blenda, e o Wurzita. Em ambos os íons minimizam as repulsões entre íons iguais.
O zinco Blenda é o mais estável em condições terrestres de pressão e temperatura; E a Wurzita, que é menos densa, resulta da reorganização cristalina devido ao aumento da temperatura.
As duas estruturas podem coexistir no mesmo ZnS sólido ao mesmo tempo, embora, muito lentamente, o Wurzita acabará predominantemente.
Zinco Blenda
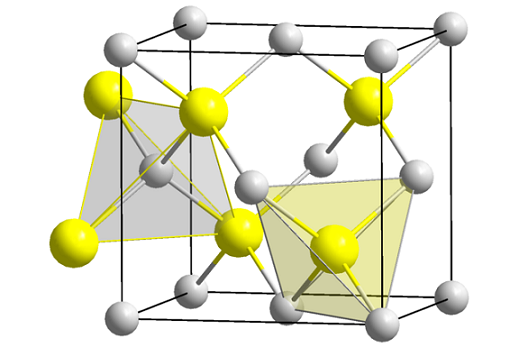
 Estrutura de Blenda de Zinco (Spheny). Fonte: Wikimedia Commons
Estrutura de Blenda de Zinco (Spheny). Fonte: Wikimedia Commons A imagem superior mostra a célula cúbica centrada nas faces da estrutura de blenda de zinco. As esferas amarelas correspondem aos ânions S2-, e cátio cinza para Zn2+, localizado nos cantos e nos centros dos rostos do cubo.
Pode atendê -lo: Isobutil: Nomenclatura, treinamento, estrutura e característicasObserve as geometrias tetraédricas ao redor dos íons. O zinco Blenda também pode ser representado por esses tetraedros, cujos orifícios dentro do vidro têm a mesma geometria (Hollows tetraedral).
Além disso, a proporção de ZnS é atendida dentro das células unitárias; isto é, uma proporção 1: 1. Assim, para cada cátion Zn2+ Há um ânion s2-. Na imagem, pode parecer que as esferas cinza abundam, mas na realidade quando estão nos cantos e no centro das faces do cubo, são compartilhadas por outras células.
Por exemplo, se as quatro esferas amarelas que estão dentro da caixa são tomadas, as “peças” de todas as esferas cinza ao redor devem adicionar o mesmo (e fazê -lo), quatro. Assim, na célula unitária cúbica, existem quatro Zn2+ e quatro s2-, A proporção estequiométrica do ZNS é cumprida.
Da mesma forma, é importante enfatizar que existem orifícios tetraédricos para a frente e atrás das esferas amarelas (o espaço que as separa uma da outra).
Wurzita
 Estrutura de wurzita. Fonte: Wikimedia Commons
Estrutura de wurzita. Fonte: Wikimedia Commons Ao contrário da estrutura da mistura de zinco, o Wurzita adota um sistema cristalino hexagonal (imagem superior). Isso é menos compacto, então o sólido tem menos densidade.
Os íons no Wurzita também têm ambientes tetraédricos e uma proporção 1: 1 que concorda com a fórmula do ZNS.
Propriedades do sulfeto de zinco
Cor
Pode ser apresentado de três maneiras:
-O Wurtzita, de cristais brancos e hexagonais.
-O Sphenhell, de cristais brancos e cristais cúbicos.
-Como um pó branco a acinzentado ou amarelado e cristais amarelados cúbicos.
Ponto de fusão
1.700 ° C.
Solubilidade em água
Praticamente insolúvel (0,00069 g/100 ml a 18 ° C).
Solubilidade
Insolúvel em álcalis, solúvel em ácidos minerais diluídos.
Densidade
Esferas 4,04 g/cm3 e Wurtzita 4,09 g/cm3.
Dureza
Tem uma dureza de 3 a 4 na escala MOHS.
Estabilidade
Ao conter a água oxida lentamente o sulfato. Em um ambiente seco, é estável.
Decomposição
Quando aquecido a altas temperaturas, ele emite vapores tóxicos de zinco e óxidos sulfurosos.
Pode atendê -lo: hidreto de sódio (NAH): propriedades, reatividade, riscos, usosNomenclatura do sulfeto de zinco
A configuração eletrônica do Zn é [AR] 3D104s2. Ao perder os dois elétrons do orbital 4s, é como o zn cation2+ Com seus orbitais de pleno. Portanto, desde eletronicamente o Zn2+ É muito mais estável que o Zn+, Tem apenas uma valência de +2.
Portanto, é omitido para a nomenclatura de ações, acrescentando sua valência fechada entre parênteses e com números romanos: sulfeto de zinco (II).
Nomenclaturas sistemáticas e tradicionais
Mas existem outras maneiras de chamar Zns, além da que já foi criada. No sistema sistemático, o número de átomos de cada elemento é especificado com os numeradores gregos, com a única exceção do elemento à direita quando é apenas um. Assim, o ZNS é nomeado como: BUNsulfeto de zinco (e não monozincon monossulfuro).
Em relação à nomenclatura tradicional, ao zinco ao ter uma única valência de +2, é adicionada adicionando o sufixo -co. Consequentemente, seu nome tradicional é: sulfeto de zíncico.
Usos de sulfeto de zinco
Como pigmentos ou revestimentos
Sachtolith
O Sachtholith é um pigmento branco feito com sulfeto de zinco. É usado em putties, mastiques, selantes, tampas inferiores, tintas de látex e sinalização.
Seu uso combinado com pigmentos absorventes de luz ultravioleta, como micro titânio ou pigmentos de óxido de ferro transparente, é necessário em pigmentos resistentes ao clima.
Zns e pinturas de látex
Quando o ZNS é aplicado em látex ou pinturas texturizadas, ele tem uma ação prolongada de microbicidas.
Janelas e quadros de aeronaves
Devido à sua grande dureza e resistência à quebra, erosão, chuva ou poeira, isso o torna adequado para janelas infravermelhas externas ou nos quadros de aeronaves.
Revestimento e outros usos
O ZNS é usado no revestimento de rotores usados no transporte de compostos, para reduzir o desgaste. Além disso, é usado na produção de tintas impressas, compostos isolantes, pigmentação termoplástica, plásticos resistentes a chamas eletroluminescentes e lâmpadas.
Pode servir a você: TunSen mais leve: características, funções, exemplos de usoDispositivos e telas de visão noturna
-O sulfeto de zinco pode ser transparente, sendo capaz de ser usado como uma janela para óptica visível e óptica infravermelha. É usado em dispositivos de visão noturna, em telas de televisão, telas de radar e revestimentos fluorescentes.
Eletroluminescência
ZnS doping com Cu é usado na produção de painéis de eletroluminescência. Além disso, é usado em propulsão de foguetes e gravimetria.
Por sua fosforescência
Sua fosforescência é usada para tingir as agulhas do relógio e, assim, visualizar o tempo no escuro; Também em pinturas para brinquedos, sinais de emergência e avisos de trânsito.
A fosforescência permite o uso de sulfeto de zinco nos tubos de raios catódicos e nas telas de raios X brilharem em pontos escuros. A cor da fosforescência depende do ativador usado.
Semicondutor, fotocatização e catalisador
- O Spheny e o Wurtzite são semicondutores de fenda de banda larga. O Sphalerite tem uma fenda de banda de 3,54 eV, enquanto o Wurtzita tem um bit de banda de 3,91 eV.
- O ZNS é usado na preparação de um fotocatalisador composto por CDS - ZNS/Zircônio - fosfato de titânio, usado para produção de hidrogênio sob luz visível.
- Intervém como um catalisador para a degradação de poluentes orgânicos. É usado na preparação de um sincronizador de cores em lâmpadas LED.
- Seus nanocristais são usados para detecção de proteínas ultrassensíveis. Por exemplo, emitindo pontos quânticos de Zns. É usado na preparação de um fotocatalisador combinado (CDS/ZNS) -TIO2 para produção elétrica via fotoeletrocatálise.
Referências
- PubChem (2018). Sulfeto de zinco. Retirado de: PubChem.NCBI.Nlm.NIH.Gov
- Quiminet (16 de janeiro de 2015). Pigmento branco baseado em sulfeto de zinco. Recuperado de: quiminet.com
- Wikipedia (2018). Sulfeto de zinco. Retirado de: em.Wikipedia.org
- II-VI UK (2015). Sulfeto de zinco (ZnS). Retirado de: II-VI.é
- Rob Toreki (30 de março de 2015). A estrutura de zincblenda (ZnS). Retirado de: Ilpi.com
- Química Librettexts (22 de janeiro de 2017). Blenda de estrutura-zinco (ZnS). Tirado de: química.Librettexts.org
- Reade (2018). Sulfeto de sulfeto/ zinco (ZnS). Retirado de: Reade.com

