Raios anódicos
- 802
- 148
- Pete Wuckert
 Tubo de raio anódico
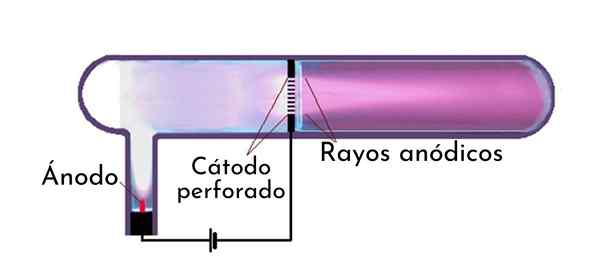
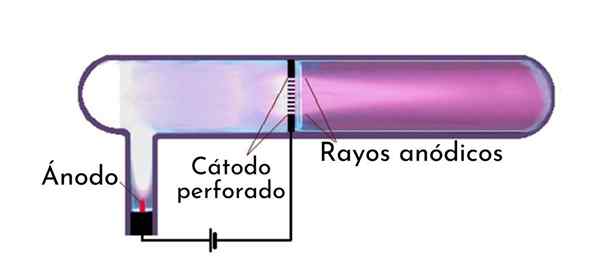
Tubo de raio anódico O que são raios anódicos?
O Raios anódicos ou raios de canal, Também chamado de positivo, são raios positivos constituídos por cátions atômicos ou moleculares (íons de carga positiva) que são direcionados para o eletrodo negativo em um tubo de Crookes.
Os raios anódicos se originam quando os elétrons que variam do cátodo ao ânodo colidem com o gás bloqueado no tubo de Crookes.
Como as partículas do mesmo sinal são repelidas, os elétrons que vão para o ânodo rasgam os elétrons presentes no córtex dos átomos de gás em seu caminho.
Assim, os átomos que foram carregados positivamente - ou seja, foram transformados em íons positivos (cátions) - são atraídos pelo cátodo (com carga negativa).
Descoberta
Foi o físico alemão Eugen Goldstein que os descobriu, observando -os pela primeira vez em 1886.
Posteriormente, o trabalho realizado nos raios anódicos pelos cientistas Wilhelm Wien e Joseph John Thomson acabaram assumindo o desenvolvimento de espectrometria de massa.
Propriedades de raios anódicos
As principais propriedades dos raios anódicos são os seguintes:
- Eles têm uma carga positiva, sendo o valor de sua carga múltipla completa da carga de elétrons (1,6 ∙ 10-19 C).
- Eles se movem em uma linha reta na ausência de campos elétricos e campos magnéticos.
- Eles se desviam na presença de campos elétricos e campos magnéticos, movendo -se em direção à área negativa.
- Eles podem penetrar nas camadas de metal finas.
- Eles podem ionizar gases.
- Tanto a massa quanto a carga das partículas que compõem os raios anódicos varia de acordo com o gás bloqueado no tubo. Normalmente sua massa é idêntica à massa dos átomos ou moléculas das quais derivam.
Pode servir a você: Soma dos vetores: método gráfico, exemplos, exercícios resolvidos- Eles podem causar mudanças físicas e químicas.
Um pouco de história
Antes da descoberta dos raios anódicos, ocorreu a descoberta dos raios do cátodo, que ocorreu ao longo dos 1858 e 1859. A descoberta é devida a Julius Plücker, matemático e físico de origem alemã.
Posteriormente, foi o físico inglês Joseph John Thomson que estudou em profundidade o comportamento, as características e os efeitos dos raios de cátodo.
 Joseph John Thomson
Joseph John Thomson Por sua parte, Eugen Goldstein - que já havia conduzido outras investigações com os raios do cátodo - foi quem descobriu os raios anódicos. A descoberta ocorreu em 1886 e fez quando ele percebeu que os tubos de descarga com o cátodo perfurado também emitiu luz no final do cátodo.
Dessa maneira, ele descobriu que, além dos raios do cátodo, havia outros raios: os raios anódicos; Estes se moveram na direção oposta. Como esses raios passaram pelos orifícios ou canais no cátodo, ele decidiu chamá -los de raios de canal.
No entanto, não era ele, mas Wilhelm Wien, que mais tarde conduziu estudos extensos dos raios anódicos. Wien, junto com Joseph John Thomson, acabou estabelecendo a base da espectrometria de massa.
A descoberta de Eugen Goldstein nos raios anódicos constituiu um pilar fundamental para o desenvolvimento subsequente da física contemporânea.
Graças à descoberta de raios anódicos, foi pela primeira vez que os enxames de átomos de movimento rápido e ordenado, cuja aplicação foi muito fértil para diferentes ramos da física atômica.
O tubo de raio anódico
Na descoberta dos raios anódicos, Goldstein usou um tubo de descarga que havia perfurado o cátodo. O processo detalhado pelo qual os raios anódicos são formados em um tubo de descarga de gás é o apresentado abaixo.
Pode atendê -lo: ondas bidimensionais
Ao aplicar uma grande diferença de potencial de vários milhares de volts no tubo, o campo elétrico que cria o pequeno número de íons que está sempre presente em um gás e que são criados por processos naturais, como a radioatividade.
Esses íons acelerados colidem com átomos de gás, iniciando elétrons e criando mais íons positivos. Por sua vez, esses íons e elétrons atacam novamente mais átomos, criando mais íons positivos no que é uma reação em cadeia.
Os íons positivos são atraídos para o cátodo negativo e alguns passam pelos buracos no cátodo. Quando chegam ao cátodo, eles já aceleraram a velocidade suficiente como, quando colidem com outros átomos e moléculas de gás, excitam espécies a níveis mais altos de energia.
Quando essas espécies retornam aos seus níveis de energia originais, átomos e moléculas liberam a energia que haviam obtido anteriormente; A energia é emitida em forma de luz.
Esse processo de produção de luz, chamado fluorescência, causa a aparência de um brilho na região onde os íons emergem do cátodo.
O próton
Enquanto Goldstein, com seus experimentos com os raios anódicos, obteve prótons, a verdade é que não é para quem é atribuído à descoberta do próton, já que ele não foi capaz de identificá -lo corretamente.
O próton é a partícula mais leve das partículas positivas que ocorrem nos tubos de raios anódicos. O próton ocorre quando o tubo é carregado com gás de hidrogênio. Dessa forma, quando o hidrogênio é ionizado e perde seus elétrons, os prótons são obtidos.
Você pode atendê -lo: terceira lei de Newton: pedidos, experimentos e exercíciosO próton tem uma massa de 1,67 ∙ 10-24 g, quase o mesmo que o átomo de hidrogênio, e tem a mesma carga, mas como um sinal que o elétron; isto é, 1.6 ∙ 10-19 C.
Espectrometria de massa
 Frente do espectrômetro de massa
Frente do espectrômetro de massa A espectrometria de massa, desenvolvida a partir da descoberta de raios anódicos, é um procedimento analítico que permite estudar a composição química das moléculas de uma substância baseada em sua massa.
Permite muito reconhecer compostos desconhecidos, compostos de contagem conhecidos, além de conhecer as propriedades e a estrutura de uma molécula de substância.
Por sua parte, o espectrômetro de massa é um dispositivo com o qual a estrutura de diferentes compostos químicos e isótopos pode ser analisada com muita precisão.
O espectrômetro de massa permite separar os núcleos atômicos com base na relação entre a massa e a carga.

