Características da proteinase K, atividade enzimática, aplicações
- 2313
- 35
- Pete Wuckert
O proteina k É uma enzima que pertence ao grupo de proteases serinas, ou seja, tem em seu centro catalítico ativo um aminoácido serina e tem a função de quebrar as ligações peptídicas por hidrólise. Por sua vez, esta enzima pertence à família de proteínas subtilisina (Peptidase S8).
A k proteinase tem um peso molecular (PM) de 28.900 daltons e foi primeiro isolado em 1.974 em extratos de fungos Álbum Engyodontium, anteriormente conhecido como o nome de Álbum Tritirachium Limber.
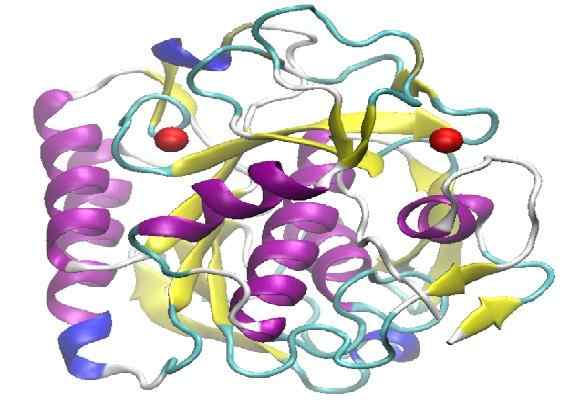
 Estrutura molecular da k proteinase. Fonte: Lykchiniadis [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)]
Estrutura molecular da k proteinase. Fonte: Lykchiniadis [CC BY-SA 4.0 (https: // CreativeCommons.Org/licenças/BY-SA/4.0)] Apresenta uma alta capacidade proteolítica, demonstrada ao ser capaz de degradar a queratina presente no cabelo. A palavra queratina em inglês está escrita "Keratin", a partir daí vem que foi chamada de "proteinsa k".
Devido ao seu alto poder para dividir as proteínas nativas, essa enzima é útil em várias técnicas de biologia molecular. Usado principalmente para isolar e preparar ácidos nucleicos com alto peso molecular (PM).
A proteinase K atua liberando o DNA nuclear, destruindo proteínas e inativo para rnases e dnate, ou seja, elimina nucleas nas preparações de DNA e RNA.
Por outro lado, foi visto que a K proteinase pode hidrolisar algumas proteínas nativas desnaturadas, o que fez do interesse dos pesquisadores para uso no estudo das proteínas príon (PRPC).
No entanto, apesar de seu alto poder proteolítico, existem proteínas resistentes à ação da proteína K. Entre eles, existem algumas proteínas anômalas chamadas príons (PRPSC), associadas a encefalopatias espongiformes transmissíveis.
[TOC]
Características da proteinase K
A k proteinase possui uma estrutura terciária composta por três camadas, com uma folha β de sete cadeias médicas entre duas camadas de hélices. Por pertencer à família de Peptidases S8 é caracterizado por apresentar uma tríade catalítica em seu local ativo, cuja ordem seqüencial é (asp, a dele e o ser), que as diferencia de outras famílias peptidase.
Pode atendê -lo: aminoácidos de proteínaEsta enzima do grupo de protease serina é caracterizada por ligações peptídicas hidrolisantes próximas ao grupo carboxílico de aminoácidos alifáticos e aromáticos.
Por outro lado, é capaz de agir na presença de certas substâncias corrosivas, como dodecilsulfato de sódio (SDS), Tris-HCl e EDTA, que são usados para ajudar a desnaturação de proteínas, fazendo com que eles perdessem sua estrutura nativa.
Esta é uma etapa anterior na preparação de proteínas para a técnica de eletroforese. A faixa de pH para a qual o k proteinsa ate é bastante amplo (2.0 a 12.0), com um pH ideal entre 7.5 a 12.0, e seu ponto isoelétrico é 8.9. Como pode ser visto, é ativo contra uma ampla gama de pH.
Outra característica que se destaca na proteinase K é sua estabilidade na presença de altas temperaturas (50 - 60 ° C).
Atividade enzimática
O k proteinsa precisa da presença de íons de cálcio, embora não afete sua atividade, se for essencial manter sua estabilidade.
Para que o K Proteinsa realize a digestão completa do substrato, é necessário um tempo de contato aproximado entre 5 minutos até 2 horas.
No entanto, nesse sentido, Daza e colaboradores compararam a pureza do DNA obtido em vários tempos de exposição contra a k proteinase e concluiu que uma incubação prolongada (até 24 h) melhora significativamente a qualidade do DNA.
Agora, em relação à concentração usada da enzima k proteinase nos diferentes protocolos, pode -se dizer que é muito variada.
Pode ser usado de concentrações muito baixas (5 µg/ml) a 500 µg/ml de concentrações. Mas as concentrações de trabalho mais frequentes variam entre 50-100μg /ml, especialmente para digestão de proteínas e nucleas. Embora para tratamento de tecidos, seja necessária uma concentração de 2 mg/ml.
Pode atendê -lo: Easmotherium sibiricum: características, habitat, fósseisFormulários
Suas aplicações são muito amplas e podem ser resumidas a seguir:
-É usado na digestão de proteínas e na extração de DNA por vários métodos, como: salga, pk-sds, cetil-tritetil amônio (CTAB), acetato de potássio modificado e acetato de extração de iodeto de sódio e acetato.
-Inativação de nucleasas (rnasas e dnasas).
-Na técnica de hibridação No local (Ele), para ajudar a liberação de ácido nucleico, além de eliminar proteínas indesejáveis.
-Modificação de proteínas.
-No nível de pesquisa, em vários estudos.
Vantagens da k proteinase
Vários estudos comparativos foram realizados entre técnicas de extração de DNA que usam k proteinase, com outros que não o usam e todos concluem que existem maiores benefícios quando a enzima é usada. Entre as vantagens, o seguinte pode ser mencionado:
-O DNA de alta qualidade, alta qualidade e pureza é obtido.
-O DNA extraído é estável por até 3 meses.
O DNA extraído pode ser usado nas seguintes técnicas: Southern blot, reação em cadeia da polimerase (PCR), eletroforese, entre outros.
Proteínas K resistentes à proteinase
Várias investigações concluíram que os príons (proteínas anômalas tóxicas de PRPSC diferem das proteínas PRPC (nativas) por serem resistentes à ação da k proteinase, enquanto os PRPCs são sensíveis à sua ação.
Outros autores descreveram que, na estrutura do prpSC, existem porções sensíveis e outras resistentes à proteinase k. No entanto, ambas as partes são igualmente tóxicas e infecciosas.
Por outro lado, Bastian e colaboradores em 1987 isolaram 4 proteínas de 28, 30, 66 e 76 kDa de uma espécie de tipo de Spiroplasma mirum. Acabou sendo resistente à ação da k proteinase e também teve uma reação cruzada com alguns príons.
Pode atendê -lo: quimiotoxisSabe -se que esta espécie pode causar cataratas importantes e danos neurológicos e, devido às descobertas científicas de Bastian, entre outras pesquisas, tentou se relacionar com esse microorganismo com encefalopatias espongiformes transmissíveis transmissíveis.
No entanto, a etiologia dessa patologia neurológica degenerativa permanece atualmente atribuída a príons.
Nesse sentido, Butler e colaboradores em 1991 identificaram e caracterizaram uma classe de uma proteinase KDA de 40 kDA -resistente a duas cepas de duas cepas de Mycoplasma hyorhinis. Esse patógeno afeta os porcos, infectando seus tecidos, mas neste caso não houve reação cruzada com as prisões testadas.
Mais pesquisas são necessárias para elucidar muitas incógnitas a esse respeito.
Referências
- Bastian F, Jennings R e Gardner W. 1987. Anti-soro para proteínas de fibrila de sucata com reação cruzada com Spiroplasma mirum Proteínas de fibril. J. Clin. Microbiol. 25: 2430-2431.
- Daza C, Guillen J, King J, Ruiz V. Avaliação de um método de extração e purificação de DNA do tecido muscular fixado no formaldeído de cadáveres não identificados. Med, 2014; 22 (1): 42-49,
- Butler G, Kotani H, Kong L, Frick M, Evancho S, Stanbridge E e McGarrity G. Identificação e caracterização de proteínas resistentes à proteína K em membros da classe Mollicutes. Infecção e imunidade, 1991, 59 (3): 1037-1042
- López M, Rivera M, Viettri M, Lares M, Marrocoima A, Herrera L, et al. Comparação de dois protocolos de extração de DNA de Trypanosoma Cruzi cultivado em meio axhênico. Rev. Peru. Med. Exp. Saúde pública 2014; 31 (2): 222-227. Disponível em: Scielo.org
- Jiménez G, Villalobos M, Jiménez E e Palma W. Determinação da eficácia de cinco protocolos de extração de DNA a partir de material parafinado para estudos moleculares. Rev Méd Medic Costa Rica. 2007; 1 (1): 10-19.
- « Flora e fauna de Santiago del Estero Espécies Principais
- História da obsolescência programada, tipos, consequências »

