Estrutura química de Pencanona, propriedades, síntese, usa
- 1947
- 372
- Dennis Heidenreich
O Pentanona É um composto orgânico, pertencente à família das cetonas, cuja fórmula química é c5H10QUALQUER. Continua sendo uma das cetonas mais simples e consiste em um líquido incolor com um aroma semelhante ao da acetona. De agora em diante, com relação ao número de carbono de seu esqueleto, as cetonas presentes na posição Isômero.
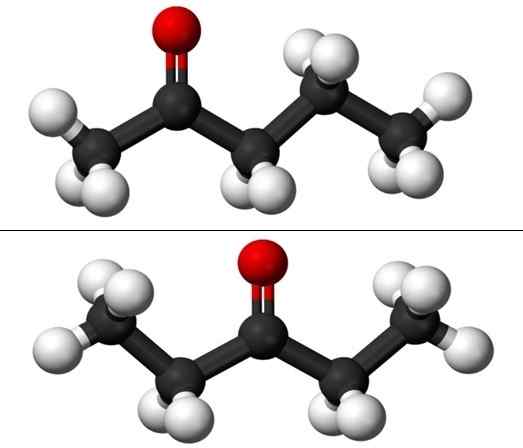
Ao falar sobre posição isomeria refere -se a onde está o grupo carbonil, c = o. Assim, Puntanona realmente consiste em dois compostos com propriedades físicas que diferem apenas uma da outra: 2 penone e 3 penone (imagem inferior). Ambos são líquidos, mas seus pontos de ebulição são os mesmos, então não podem ser separados por destilação.
 Moléculas da posição isômeros para Pentanona. Fonte: Jynto e Ben Mills via Wikipedia.
Moléculas da posição isômeros para Pentanona. Fonte: Jynto e Ben Mills via Wikipedia. No entanto, cada uma das duas pentanonas tem sua própria rota de síntese, por isso é improvável que haja uma mistura delas; mistura que pode ser viável para separar por congelamento.
Seus usos são restritos especialmente como solventes orgânicos; Alternativas à acetona na mídia, onde você trabalha com uma temperatura superior ao seu ponto de ebulição baixo. Eles também são materiais de partida para outra síntese orgânica, pois seu grupo C = O pode reduzir ou sofrer adição nucleofílica.
[TOC]
Estrutura química
Isômeros de posição
Na imagem, temos as estruturas moleculares dos dois isômeros de posição para os Puntanona, representados por um modelo de esferas e barras. As esferas pretas correspondem a esqueletos carbonatados, átomos brancos a hidrogênio e átomos de oxigênio vermelho no grupo C = O.
2-Pintanona
O 2-Ponanona (acima) possui grupo C = ou no segundo carbono, que é equivalente a se estivesse na sala; isto é, o 2-Ponanona e o 4-Pantanona são equivalentes, pois é suficiente para girá-los 180º para que suas estruturas sejam iguais.
Pode atendê -lo: tetracloreto de carbono (CCL4)À esquerda de c = o, você tem um radical metilo, CHO3-, E à sua direita, uma propila radical. É por isso que esse Cetona também recebe o nome (menos usado) do Metil Profil Cetona (MPK em inglês). Você pode ver a assimetria dessa estrutura à primeira vista.
3-penone
O 3-Péntanona (abaixo) tem o grupo C = O no terceiro carbono. Observe que este isômero é uma versão maior da acetona e que também é muito simétrica; Os dois radicais nas laterais do grupo C = O são iguais: dois radicais de etila, CH3CH2-. É por isso que o 3-Pananona também é chamado Cetona Diestil (ou dimetil acetona).
Interações intermoleculares
A presença do grupo carbonil, tanto na 2-pantanona quanto no 3-Penona, confere polaridade à molécula.
Portanto, ambos os isômeros Pentanona são capazes de interagir entre si através do dipolo-dipol.
Da mesma forma, as forças de dispersão de Londres entre carbono e esqueletos hidrogenados intervêm em menor grau.
Por ter o Puntanona, uma área molecular e massa maior em comparação com as da acetona, essa contribuição aumenta seu momento dipolar e permite um ponto de ebulição mais alto (102 ºC> 56 ºC) possuir um ponto de ebulição mais alto). De fato, os dois isômeros vaporizam a 102 ºC; Enquanto eles congelam em diferentes temperaturas.
Cristais
Provavelmente na cristalização, as simetrias desempenham um papel importante. Por exemplo, o ponto de fusão do 2 -Pantanona é -78 ºC, enquanto o 3 -Péntanona, -39 ºC.
Pode atendê -lo: Avogadro LawIsso significa que os cristais de 3-Pantanona são mais estáveis contra a temperatura; Suas moléculas são mais coesas e requerem mais calor para se separar na fase líquida.
Se houvesse uma mistura de ambos os isômeros, o 3 penone seria o primeiro a cristalizar, finalmente sendo o 2-Pananona a uma temperatura mais baixa. As moléculas da 3-pantanona, mais simétricas, são orientadas mais facilmente do que as de 2-Ponanona: assimétricas e ao mesmo tempo mais dinâmicas.
Propriedades
Aparência física
Líquidos incolores com um aroma semelhante ao da acetona.
Massa molar
86,13 g/mol
Densidade
0,81 g/ml (3-Ponanona)
0,809 g/ml (2-Ponanona)
Ponto de fusão
-78 ºC (2-Ponanona)
-39 ºC (3-Ponanona)
Ponto de ebulição
102 ºC (para ambos os isômeros)
Solubilidade em água
35 g/L (3-Ponenona)
60 g/L (2-Ponenona)
Pressão de vapor
35 MMHG (3-Ponenona)
270 mmHg (2-pantanona) a 20 ºC
Esses valores não são úteis para comparar diretamente as pressões de vapor de ambos os isômeros, pois o primeiro é relatado sem a temperatura em que foi medido.
ponto de inflamação
12,78 ºC (3-Ponanona)
10 ºC (2-Ponanona)
Estabilidade
Os dois isômeros de Pentanona são extremamente inflamáveis, então devem permanecer o mais longe possível de qualquer fonte de calor. Os pontos de flash indicam que uma chama pode definir os vapores de ambas as pentanas, mesmo a uma temperatura de 10 ºC.
Síntese
Embora os dois isômeros de Pentanona sejam fisicamente e quimicamente muito semelhantes, suas rotas sintéticas são independentes do outro, por isso é improvável que ambos sejam obtidos na mesma síntese.
2-Pintanona
A partir do reagente 2-penol, um álcool secundário, isso pode ser oxidado em 2-Ponanona usando ácido hipocloroso formado in situ, HCLO, como um agente oxidante. A oxidação seria:
Pode atendê -lo: sem eletrólitos: características e exemplos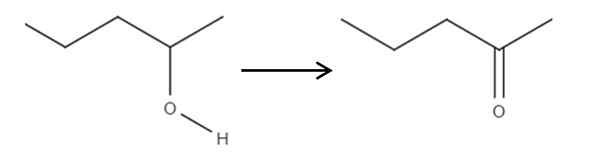 Oxidação de 2-pantanol a 2-pantanona. Fonte: Gabriel Bolívar.
Oxidação de 2-pantanol a 2-pantanona. Fonte: Gabriel Bolívar. Simplesmente o link C-OH se torna C = O. Existem outros métodos para sintetizar o 2-Penona, mas este é o mais simples de entender.
3-penone
A 3-Pintanona pode ser sintetizada por meio3CH2COOH. Esta rota sintética produz cetonas simétricas e é uma molécula de CHO3O COOH perderá o grupo COOH na forma de CO2, Enquanto o outro seu grupo oh na forma de H2QUALQUER:
2CH3CH2COOH => CH3CH2Coch2CH3 + Co2 + H2QUALQUER
Outra rota um pouco mais complexa é reagir diretamente uma mistura de etileno, CHO2= Cap2, Co2 e h2 Para formar o 3-Ponanona.
Formulários
A menos que o aplicativo seja muito rigoroso, é uma síntese específica, ou que também foi demonstrado que os dois isômeros não causam os mesmos resultados, é irrelevante escolher entre usar a 2 penona ou 3 penona em qualquer um de seus usos.
Ou seja, "não importa" se você quiser usar o 2-Ponanona ou 3-Penona como um solvente de pinturas ou resinas, ou como um miserável, porque os critérios mais importantes se tornarão seu preço e disponibilidade. A 3 penona é usada na indústria automotiva para estudar o comportamento de gases dentro dos motores de combustão interna.
Referências
- Morrison, r. T. e boyd, r, n. (1987). Quimica Organica. 5ª edição. Interamericano Editorial Addison-Wesley.
- Carey f. (2008). Quimica Organica. (Sexta edição). Mc Graw Hill.
- Graham Solomons t.C., Craig b. Fryhle. (2011). Química orgânica. Aminas. (10ª edição.). Wiley Plus.
- Wikipedia. (2019). 3-pain. Recuperado de: em.Wikipedia.org
- Centro Nacional de Informações sobre Biotecnologia. (2019). 2-Pontenona. Banco de dados PubChem. CID = 7895. Recuperado de: pubchem.NCBI.Nlm.NIH.Gov
- Sociedade Real de Química. (2019). 3-pain. Recuperado de: chemspider.com
- Professor T. Nalli. (2013). Oxidação de 2-Pintanol e destilação do produto. Recuperado de: curso1.Winona.Edu
- « História e significado da bandeira do Paraguai
- História e significado da bandeira do Reino Unido »

