Características de lisina, estrutura, funções, biossíntese
- 3751
- 523
- Dennis Heidenreich
O lisina (Lys, K) ou o Ácido ε-diaminoproóico, É um dos 22 aminoácidos que fazem.
Foi descoberto por Drechsel em 1889 como um produto da hidrólise (decomposição) do caseinogênio. Anos depois, Fischer, Siegfried e Hedin determinaram que também fazia parte de proteínas como gelatina, albumina de ovo, conglutina, fibrina e outras proteínas.
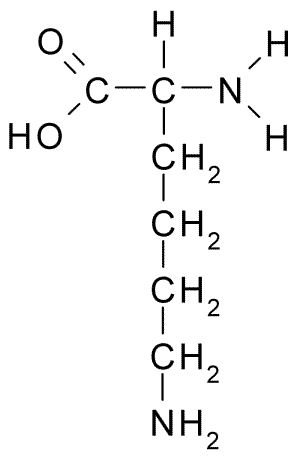
 Estrutura química da lisina de aminoácidos (fonte: Borb, via Wikimedia Commons)
Estrutura química da lisina de aminoácidos (fonte: Borb, via Wikimedia Commons) Sua ocorrência foi então demonstrada em mudas de sementes na germinação e na maioria das proteínas vegetais examinadas, o que determinou sua abundância como um elemento constituinte geral de todas as proteínas celulares.
É considerado um dos principais aminoácidos "limitantes" das dietas ricas em cereais e, por esse motivo.
Alguns estudos determinaram que a ingestão de lisina favorece a produção e a liberação de hormônios de insulina e glucagon, que têm efeitos importantes no metabolismo energético do corpo.
[TOC]
Caracteristicas
Lisina é um α-aminoácido carregado positivamente.53, o que implica que, pH fisiológico, seu grupo amino substituinte é completamente ionizado, conferindo uma carga líquida positiva ao aminoácido.
Sua ocorrência em proteínas de diferentes tipos de organismos vivos é próxima de 6% e vários autores consideram que a lisina é essencial para o crescimento e reparo adequados dos tecidos.
As células têm muitos derivados de lisina, que cumprem uma grande diversidade de funções fisiológicas. Nestes estão hidroxilisina, metil-lisina e outros.
É um aminoácido cetogênico, o que implica que seu metabolismo produz esqueletos carbonatados de substratos intermediários para rotas de formação de moléculas, como acetil-CoA, com a formação subsequente de corpos de cetona no fígado.
Ao contrário de outros aminoácidos essenciais, este não é um aminoácido glicogênico. Em outras palavras, sua degradação não termina com a produção de rotas intermediárias que produzem glicose.
Estrutura
A lisina é classificada dentro do grupo de aminoácidos básicos, cujas cadeias laterais têm grupos ionizáveis com cargas positivas.
Sua cadeia lateral ou grupo R R possui um segundo grupo primário de amino ligado ao átomo de carbono na posição ε de sua cadeia alifática, daí seu nome “ε-aminocaproico”.
Possui um átomo de carbono α, para o qual um átomo de hidrogênio, um grupo amino, um grupo carboxil e a cadeia lateral R R, caracterizada pela fórmula molecular (-CH2-CH2-CH2-CH2-NH3+).
Como a cadeia lateral possui três grupos de metileno e, embora a molécula de lisina tenha um grupo amino com carga positiva ao pH fisiológico, esse grupo r tem um forte caráter hidrofóbico, por isso é frequentemente "enterrado" nas estruturas proteicas, deixando apenas o ε- grupo amino.
O grupo amino da cadeia lateral da lisina é altamente reativo e, geralmente participa dos centros ativos de muitas proteínas com atividade enzimática.
Funções
A lisina, sendo um aminoácido essencial, cumpre várias funções, como micronutrientes, especialmente em humanos e outros animais, mas também é metabólito em diferentes organismos, como bactérias, leveduras, plantas e algas.
As características de sua cadeia lateral, especificamente as do grupo ε-amino ligadas à cadeia de hidrocarbonetos que é capaz de formar pontes de hidrogênio, proporcionam propriedades especiais que o fazem participar de reações catalíticas em vários tipos de enzimas.
Pode atendê -lo: flora e fauna de Zacatecas: espécies mais representativasÉ muito importante para o crescimento normal e a remodelação dos músculos. Além disso, é uma molécula precursora para a carnitina, um composto sintetizado no fígado, cérebro e rins responsáveis pelo transporte de ácidos graxos para mitocôndrias para produção de energia.
Este aminoácido também é necessário para a síntese e a formação de colágeno, uma importante proteína do sistema de tecido conjuntivo no corpo humano, por isso contribui para a manutenção da estrutura da pele e dos ossos.
Ele reconheceu experimentalmente funções em:
- A proteção dos intestinos contra estímulos estressantes, contaminação com patógenos bacterianos e virais, etc.
- Diminuir os sintomas de ansiedade crônica
- Favorecer o crescimento de bebês que crescem sob dietas de baixa qualidade
Biossíntese
Os seres humanos e outros mamíferos não podem sintetizar o aminoácido lisina Na Vivo E é por esse motivo que eles devem obtê -lo de proteínas animais e vegetais ingeridas com alimentos.
No mundo natural, duas rotas diferentes evoluíram para a biossíntese de lisina: uma que usa bactérias, plantas e fungos "mais baixo" e outro usado por Euglénides e fungos "superiores".
Biossíntese de lisina em plantas, fungos mais baixos e bactérias
Nesses organismos, a lisina é obtida do ácido diamineopimélico através de uma rota de 7 etapas que começam com piruvato e semi -o aspartato ético. Para bactérias, por exemplo, essa rota implica a produção de lisina com fins de (1) síntese proteica, (2) síntese de diaminopimelado e síntese de (3) lisina que será usada na parede celular de pepidoglin.
O aspartato, em organismos que apresentam essa rota, não apenas dá origem a Lisina, mas também deriva na produção de metionina e treonina.
A rota divergente no semiiard Asp.
Biossíntese de lisina em fungos superiores e euglénidos
Síntese de lisina de Novo Em Fungos superiores e microorganismos de Euglénid, ocorre através do intermediário L-α-aminoadipato, que é transformado inúmeras vezes de maneiras diferentes daqueles que ocorrem em bactérias e plantas.
A rota consiste em 8 etapas enzimáticas, que envolvem 7 intermediários livres. A primeira metade da rota ocorre nas mitocôndrias e alcança a síntese de α-aminoadipato. A conversão de α-aminoadipato em l-lisina ocorre posteriormente no citosol.
- A primeira etapa da rota consiste na condensação das moléculas de α-cetoglutarato e acetil-CoA pela enzima homocitrato de homocitrato de sintase, que produz ácido homocítrico.
- O ácido homocírio é desidratado em ácido Cis-Homoaconítico, que é então convertido em ácido homoisocítico por uma enzima homoaconitasa.
- O ácido homoisocítrico é oxidado pela homoisocitrato desidrogenase, que alcança a formação transitória de oxiglarato, que perde uma molécula de dióxido de carbono (CO2) e termina como α-catoadipic ácido.
- Este último composto é transaminado por um processo dependente de glutamato graças à ação da enzima aminoadipada aminotransferase, que produz ácido L-α-aminoadípico.
- A cadeia lateral do ácido L-α-aminoadípico é reduzida para formar L-α-aminoadipic-δ-MEMI-ASSESSO.
- Sacoopine redutase então catalis. Posteriormente, o imino é reduzido e a sacoopina é obtida.
- Finalmente, a ligação de carbono-nitrogênio na porção de glutamato da sacaopina é "cortada" pela enzima sacraopina desidrogenase, rendendo-se como produtos finais L-lisina e α-zetoglutarato de ácido.
Alternativas à lisina
Testes e análises experimentais realizadas com ratos em um período de crescimento permitiu elucidar que o ε-N-A acetil-lisina pode substituir a lisina para apoiar o crescimento de jovens e isso graças à presença de uma enzima: ε-lisin acilase.
Pode servir a você: Zona Affótica: Características, Flora, FaunaEsta enzima catalisa a hidrólise do ε-N-acetil-lisina para produzir lisina e o faz de maneira rápida e abundante.
Degradação
Em todas as espécies de mamíferos, o primeiro passo na degradação da lisina é catalisado pela enzima lisina-2-oxoglutarato redutase, capaz de converter lisina e α-oxoglutarato em sacalopina, um derivado aminoácido presente em líquidos fisiológicos animais e cujos cujos existentes foram demonstrados No final dos anos 60.
A sacroopina está de volta ao α-aminoadipato δ-semialdehid e glutamato por ação da enzima sacaropina desidrogenase. Outra enzima também é capaz de usar Sacaropina como substrato para Hydrolyz.
A sacaropina, um dos principais intermediários metabólicos da degradação da lisina, tem uma taxa de substituição, em condições fisiológicas, extremamente alta, por isso não se acumula em fluidos ou tecidos, que foram demonstrados pelas altas atividades encontradas da desidrogenase do desenvolvedor.
No entanto, a quantidade e atividade das enzimas envolvidas no metabolismo da lisina depende, em grande parte, em vários aspectos genéticos de cada espécie em particular, uma vez que existem variações intrínsecas e mecanismos de controle ou regulação específicos.
"Sacaropinúria"
Existe uma condição patológica relacionada à perda abundante de aminoácidos como lisina, citulina e histidina através da urina, e isso é conhecido como "Saropinúria". A sacaropina é um derivado de aminoácidos do metabolismo da lisina que é excretado junto com os três aminoácidos mencionados na urina de pacientes "Sarapinúrios".
A sacaropina foi descoberta inicialmente em leveduras de cerveja e é um precursor da lisina nesses microorganismos. Em outros organismos eucarióticos, este composto é produzido durante a degradação da lisina nas mitocôndrias dos hepatócitos
Alimentos ricos em lisina
A lisina é obtida a partir dos alimentos consumidos com a dieta e um ser humano adulto médio precisa de pelo menos 0.8 g deste dia. É encontrado em inúmeras proteínas de origem animal, especialmente em carnes vermelhas, como vaca, cordeiro e frango.
É em peixes como atum e salmão e em frutas do mar, como ostras, camarões e mexilhões. Também está presente nas proteínas constituintes de produtos lácteos e seus derivados.
Em alimentos vegetais, é encontrado nas batatas, em pimenta e alho -porro. É também em abacates, pêssegos e peras. Em legumes como feijão Arriñonados, grão de bico e soja; em sementes de abóbora, nas nozes da macadâmia e nos Anacardos (Merey, Marañón, etc).
Benefícios da sua ingestão
Este aminoácido está incluído em numerosos medicamentos para formulação nutracêutica, ou seja, isolados de compostos naturais, especialmente plantas.
É usado como anticonvulsivo e sua eficácia também foi demonstrada na inibição da replicação do Vírus herpes simplex Tipo 1 (HSV-1), que geralmente se manifesta em momentos de estresse, quando o sistema imunológico está deprimido ou "enfraquecido" como ampolas ou herpes nos lábios.
A eficácia dos suplementos de L-lisina para o tratamento do herpes labial se deve ao fato de que isso "compete" ou "bloqueia" a arginina, outro aminoácido de proteína, o que é necessário para a multiplicação de HSV-1.
Foi determinado que a lisina também tem efeitos anti-aprimorados, pois ajuda a bloquear receptores envolvidos nas respostas a diferentes estímulos estressantes, além de participar da diminuição dos níveis de cortisol, "hormônio do estresse".
Alguns estudos indicaram que pode ser útil para a inibição de tumores carcinogênicos, para a saúde dos olhos, para o controle da pressão arterial, entre outros.
Pode atendê -lo: mídia de cultura: história, função, tipos, preparaçãoEm animais
Uma estratégia comum para tratar infecções por vírus do herpes I em felinos é a suplementação de lisina. No entanto, algumas publicações científicas estabelecem que esse aminoácido não possui, em felinos, sem propriedade antiviral, mas sim diminuindo a concentração da arginina.
Na saúde dos bebês
A ingestão experimental de L-Lisina, adicionada ao leite infantil durante o período de amamentação, provou ser benéfico para o ganho de massa corporal e indução de apetite em crianças durante os primeiros estágios do desenvolvimento pós-natal.
No entanto, o excesso de L-lisina pode causar excreções urinárias exageradas de aminoácidos, características neutras e básicas, resultando em um desequilíbrio corporal deles.
O excesso de suplementação de L-lisina pode terminar na repressão do crescimento e outros efeitos histológicos óbvios em órgãos importantes, provavelmente devido à perda de aminoácidos com urina.
No mesmo estudo, também foi evidenciado que a suplementação de lisina melhora as propriedades nutricionais das proteínas vegetais ingeridas.
Outros estudos semelhantes realizados em adultos e crianças de ambos os sexos no Gana, Síria e Bangladesh, trouxeram as propriedades benéficas da ingestão de lisina para reduzir a diarréia em crianças e algumas condições respiratórias mortais em homens adultos em homens.
Distúrbios de deficiência de lisina
A lisina é, como todos os aminoácidos essenciais e não essenciais, necessários para a síntese correta de proteínas celulares que contribuem para a formação de sistemas orgânicos do corpo.
As deficiências marcantes da lisina na dieta, pois é um aminoácido essencial que não é produzido pelo corpo, pode resultar no desenvolvimento de pinturas ansiosas mediadas pela serotonina, além da diarréia, também relacionadas aos receptores de serotonina.
Referências
- Tigela, s., & Bunnik, e. M. (2015). A súplica de lisina não é efetiva para a prevenção ou tratamento da infecção felina do herpesvírus 1 em gatos: uma revisão sistemática. Pesquisa veterinária da BMC, onze(1).
- Carson, n., Scally, b., Neill, d., & Carré eu. (1968). Sacaropinúria: um novo erro inato do metabolismo da lisina. Natureza, 218, 679.
- Colina R, J., Díaz e, M., Manzanilla m, l., Araque m, h., Martínez G, G., Rossini V, M., & Jerez-Timaure, n. (2015). Avaliação dos níveis de lisina digerível em dietas com alta densidade de energia para acabar porcos. Revista MVZ Córdoba, vinte(2), 4522.
- Bolsistas, b. F. C. Yo., & Lewis, M. H. R. (1973). Metabolismo de lisina em mamíferos. Jornal Bioquímico, 136, 329-334.
- Fornazier, r. F., Azevedo, r. PARA., Ferreira, r. R., & Varisi, V. PARA. (2003). Catabolismo de lisina: fluxo, papel metabólico e regulação. Jornal brasileiro de fisiologia vegetal, quinze(1), 9-18.
- Ghosh, s., Smriga, m., Vuvor, f., Suri, d., Mohammed, h., Armah, s. M., & Scrimshaw, n. S. (2010). Efeito da súplica de lisina na saúde e morbidade em indivíduos pertencentes a famílias peri-urbanas pobres em Accra, Gana. American Journal of Clinical Nutrition, 92(4), 928-939.
- Hutton, c. PARA., Perugini, m. PARA., & Gerrard, J. PARA. (2007). Inibição da biossíntese de lisina: uma estratégia de antibióticos em evolução. Biossistemas moleculares, 3(7), 458-465.
- Kalogeropoul, d., Lafave, l., Schweim, k., Gannon, m. C., & Nuttall, f. Q. (2009). A ingestão de lisina atenua acentuadamente a resposta da glicose à glicose ingerida sem uma mudança na resposta da insulina. American Journal of Clinical Nutrition, 90(2), 314-320.
- Nagai, h., & Takeshita, S. (1961). Efeito nutricional da suplementação de L-lisina no crescimento de bebês e crianças. Pediatria japonesa, 4(8), 40-46.
- O'Brien, s. (2018). Healthline. Recuperado em 4 de setembro de 2019, da www.Healthline.com/nutrição/benefícios de lisina
- Zabriskie, t. M., & Jackson, M. D. (2000). Biossíntese e metabolismo de lisina em fungos. Relatórios de produtos naturais, 17(1), 85-97.

