Hidrocarbonetos insaturados
- 3079
- 231
- Conrad Schmidt
Explicamos o que hidrocarbonetos insaturados, sua classificação, propriedades, nomenclatura e vários exemplos são
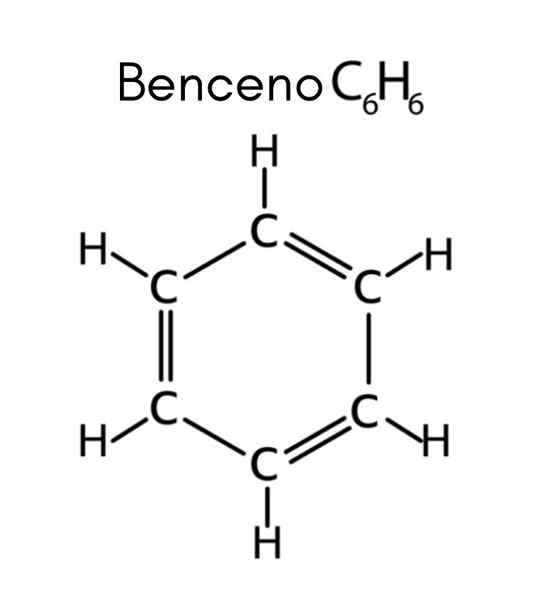
 Benzeno é um exemplo de hidrocarboneto insaturado
Benzeno é um exemplo de hidrocarboneto insaturado O que são hidrocarbonetos insaturados?
O hidrocarbonetos insaturados São compostos orgânicos formados apenas por carbono e hidrogênio, que têm uma ou mais ligações múltiplas entre átomos de carbono. Isso significa que qualquer composto de fórmula CxHe que apresentam uma ligação dupla ou tripla é um hidrocarboneto insaturado.
Os hidrocarbonetos insaturados são formados por alcenos e alcinas, bem como compostos aromáticos. A razão pela qual eles são insaturados é porque eles têm um número menor de hidrogênios do que o máximo que poderiam ter, dado o número de átomos de carbono na estrutura.
Os hidrocarbonetos insaturados são reconhecidos por ter menos de 2n+2 hidrogênios (que é o número máximo de hidrogênios que podem ser carbono), onde n é o número de átomos de carbono na fórmula molecular.
Um exemplo de hidrocarboneto insaturado é o buteno, cuja fórmula molecular é c4H8. O número máximo de hidrogênios para 4 carbonos seria 2 (4) +2 = 10 hidrogênios. Isso corresponde ao número de hidrogênios de um hidrocarboneto saturado. Como o buteno tem apenas 8 hidrogênios, que é menor que 10, é um hidrocarboneto insaturado.
O número de insaturação
Os hidrocarbonetos insaturados são caracterizados pelo número de insaturação. Isso indica que o número de pares de hidrogênio menor que um hidrocarboneto insaturado é comparado a um saturado que possui o mesmo número de carbonos.
O número de insaturação pode ser calculado para qualquer composto não saturado por meio da seguinte fórmula:
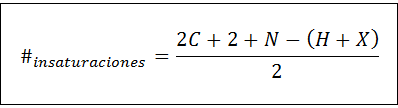
Onde c, n, h e x representam o número de carbonos, nitrogênios, hidrogênios e halogênios na fórmula molecular, respectivamente. Esse número nos dá uma idéia de quantas duplas ou títulos triplos tem um composto, dada sua fórmula molecular, embora deva ser tomada, porque os ciclos (que não são insatrição) também contribuem para o número de insaturação:

Exemplo
Benzeno tem fórmula C6H6, Portanto, o número de insaturação é:
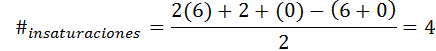
Nesse caso, a insaturação 4 corresponde a três links duplos e um ciclo.
Classificação de hidrocarbonetos insaturados
De acordo com o tipo de hidrocarboneto
- Alcenos: Eles são aqueles que têm pelo menos um link duplo em sua estrutura.
- Alkynes: Eles são aqueles que têm pelo menos um link triplo em sua estrutura.
- Aromático: São compostos poliinsaturados cíclicos com propriedades especiais que os tornam particularmente estáveis.
De acordo com a cadeia de carbono
- Linear: compostos insaturados nos quais todos os átomos de carbono estão ligados entre si em uma única cadeia.
- Ramificado: Eles são aqueles que têm uma corrente principal e também várias cadeias laterais que formam ramificações.
- Cíclico: São aqueles em que é apresentado um ciclo fechado de átomos de carbono nos quais pelo menos uma ligação dupla ou tripla é apresentada (cicloalquenos, cicloalquinos e aromático).
De acordo com o número de insaturação
- Monoinsaturado: Quando eles têm apenas um link múltiplo, ou seja, é uma única ligação dupla ou um único link triplo.
- Polynsaturado: Quando a estrutura tem mais de um link múltiplo, como no caso dos Alkian, Alkian, Alkenins, etc.
Propriedades de hidrocarbonetos insaturados
As propriedades dos hidrocarbonetos insaturados dependem fortemente do tipo específico de hidrocarboneto em questão:
Pontos de fusão e de ebulição
Em geral, hidrocarbonetos insaturados têm baixa fusão e pontos de ebulição. No entanto, em comparação com os alcanos, os alcenos com o mesmo número de carbonos e cadeia principal semelhante geralmente têm um ponto de ebulição mais baixo, enquanto os alcinos tendem a ter maiores pontos de ebulição.
O mesmo vale para pontos de fusão. Na tabela a seguir, pode-se observar que tanto o ponto de fusão quanto a ebulição do 1-penteno são inferiores aos do Pentan e aqueles que os do 1-pentino.

Estado físico
Devido a seus pontos de fusão e ebulição baixa, os hidrocarbonetos de peso de baixo peso molecular insaturados tendem a ser gasosos à temperatura ambiente. Muitos também são líquidos e os de maior peso molecular são sólidos. Em muitos casos, os sólidos são sólidos amorfos em vez de cristalino.
Polaridade
Todos os hidrocarbonetos, incluindo insaturados, são compostos apolares, porque a eletronegatividade de carbono e o hidrogênio são muito semelhantes. A única exceção é no caso de Alcines terminais2 e sp3.
Solubilidade
Sendo apolar, hidrocarbonetos insaturados são insolúveis em água e outros solventes polares, mas são muito solúveis em solventes apolares, como tetracloreto de carbono, ciclohexana e outros. De fato, muitos desses compostos são, por si só, solventes apolares.
Pode atendê -lo: disposio: estrutura, propriedades, obtenção, usosEles são combustíveis
Uma característica de todos os hidrocarbonetos, incluindo insaturados, é que eles queimam na presença de oxigênio para se tornarem dióxido de carbono e energia liberando energia na forma de luz e calor.
Eles podem polimerizar
Através de diferentes reações químicas, alcenos e alcinas podem se juntar um ao outro para formar polímeros como no caso de polietileno e polipropileno, para mencionar apenas alguns. Portanto, hidrocarbonetos insaturados são o material de partida de muitos plásticos comuns.
Reatividade química
A reatividade depende fortemente do tipo de grupo funcional que possui uma molécula. No caso de alcenos e alcinas, eles geralmente são bastante reativos e podem sofrer reações de hidrogenação, hidratação, hidrohalogenação e outros tipos de reações de adição.
Por outro lado, os compostos aromáticos geralmente são bastante inertes porque são muito estáveis. As reações características desses compostos são as reações de substituição eletrofílica aromática.
Nomenclatura de hidrocarbonetos insaturados
Nomenclatura de alcenos
Alcenos lineares
O nome dos alcenos lineares é construído colocando um prefixo que indica o número de átomos de carbono na cadeia, seguido pelo localizador de carbono, onde a ligação dupla separada começa com scripts do restante do nome e terminada com o sufixo _eno:
Prefixo-localizador
- Exemplo:
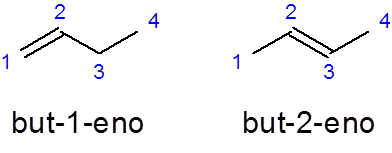
Ele Mas -1 -no É o nome do buteno linear com uma ligação dupla no primeiro carbono enquanto Mas-2-nine Tem a ligação dupla no segundo carbono.
Alcenos ramificados
No caso de alcenos ramificados, a cadeia principal mais longa que contém dois carbonos de ligação dupla é a primeira selecionada e a prioridade da ligação dupla é numerada. O nome é construído primeiro colocando as ramificações em ordem alfabética precedida por seus localizadores seguidos pelo nome da cadeia principal, conforme indicado acima.
- Exemplo:
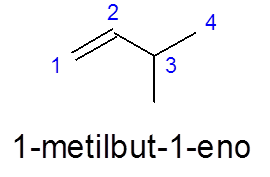
No 3-metilbut-1 -en, a numeração é feita da esquerda para a direita para dar prioridade à ligação dupla, em vez de dar prioridade à ramificação (o grupo metil).
Polienos
No caso de alcenos polienosos ou poliênicos, que contêm mais de uma ligação dupla, o maior número possível de ligações duplas é selecionado como a cadeia principal, independentemente de haver outras cadeias mais longas.
Em nome da cadeia principal, um localizador é adicionado para cada ligação dupla e o prefixo di, tri, tetra, etc. antes do término -Eno, para indicar o número de links duplos que você tem.
- Exemplo:
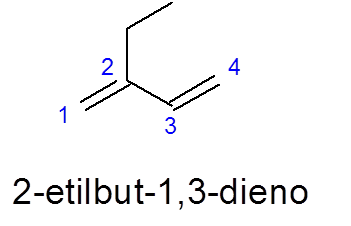
Observe que, apesar do fato de haver uma cadeia de 5 carbono mais longa, o 4 de 4 é selecionado, pois contém os dois links duplos.
Nomenclatura dos Alquinos
Os alcinos são nomeados muito semelhantes aos alcenos, com a única diferença de que o nome termina em -ino em vez de -eno. Nos casos em que há mais de um link triplo, os localizadores de todos são colocados e o prefixo numérico que indica quantos existem.
- Exemplo:
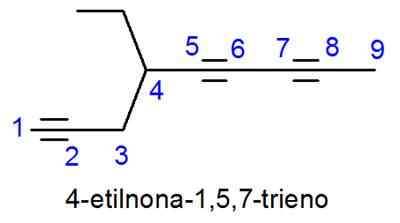
Nomenclatura de compostos aromáticos
Os hidrocarbonetos aromáticos são nomeados como derivados de benzeno e tanto a numeração quanto a maneira de nomeá -los depende de quantos substituintes o anel tem.
Anéis aromáticos com um único substituinte
Nesse caso, não é necessário. O nome consiste no nome do ramo seguido pela palavra benzeno.
- Exemplo:
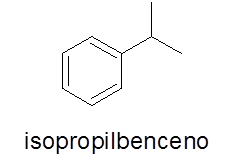
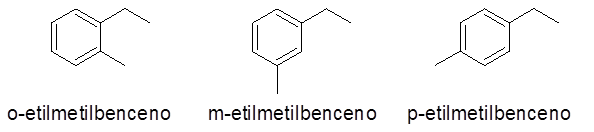
Anéis aromáticos com dois substituintes
Nesse caso, 3 números ou padrões de substituição podem ser dados (1.2), (1.3) e (1,4). Como é indiferente indicar qual substituto está no carbono 1 e que no outro, os prefixos de Ortho (O-), meta- (m-) e para- (p-), respectivamente, para se referir ao mesmo.
- Exemplos:
Anéis aromáticos com mais de 2 substituintes
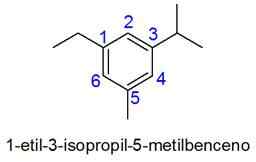
Nesse caso, a numeração da menor combinação de localizadores é selecionada. Se dois números forem iguais, é dada prioridade aos substituintes de acordo com a ordem alfabética.
- Exemplos:
Exemplos de hidrocarbonetos insaturados
Em seguida, exemplos adicionais de hidrocarbonetos insaturados são apresentados aos já mencionados.
Acetileno (c2H2)
Acetileno é o nome comum do etino, a alquimina mais simples. Este composto tem 2 insaturação devido ao seu link triplo e é usado, entre outras coisas, no equipamento de aço e soldagem.
Ciclohexeno (c6H10)
Alkeno cíclico de 6 carbono que tem duas insatação: um devido ao ciclo e o outro devido à ligação dupla.
Alongamento (c8H8)
Este composto é comumente usado na preparação dos polímeros. É um alceno aromático com 5 insatação.

