Treinamento cíclico de GMP e degradação, estrutura, funções
- 1679
- 171
- Dennis Heidenreich
Ele GMP cíclico, Também conhecido como monofosfato cíclico de guanosina, monofosfato cíclico de guanosina ou guanosina 3 ', 5'-monofosfato, é um nucleotídeo cíclico envolvido em numerosos processos celulares, especialmente aqueles relacionados à sinalização e comunicação intracelular.
Foi descrito pela primeira vez há mais de 40 anos, logo após a descoberta de seu análogo, o amplificador cíclico, que difere dela em termos da base nitrogenada, porque não é um nucleotídeo de guanina, mas de adenina.
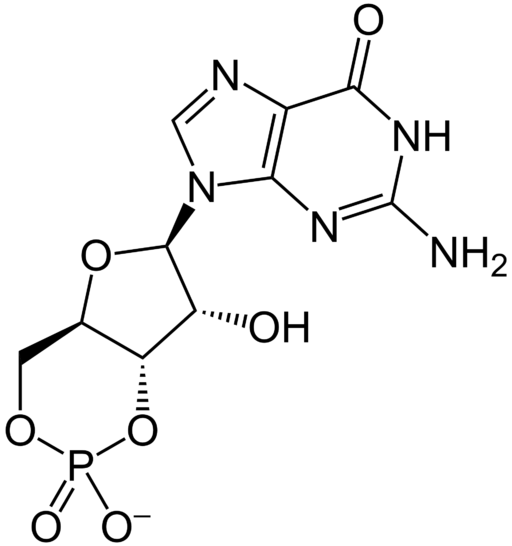
 Estrutura química do Monofosfato Cíclico de Guanosín ou GMP (Fonte: In: Usuário: Diberri [CC BY-SA 3.0 (http: // criativecommons.Org/licenças/BY-SA/3.0/)] via Wikimedia Commons)
Estrutura química do Monofosfato Cíclico de Guanosín ou GMP (Fonte: In: Usuário: Diberri [CC BY-SA 3.0 (http: // criativecommons.Org/licenças/BY-SA/3.0/)] via Wikimedia Commons) Como outros nucleotídeos cíclicos, como o AMP cíclico mencionado acima ou como CTP cíclico (monofosfato cíclico citidina), a estrutura do GMP cíclico é decisivo por suas propriedades químicas e atividade biológica, além disso, torna -o mais estável do que seu contrapartida.
Este nucleotídeo é produzido por uma enzima conhecida como Guanilil Ciclasa e é capaz de disparar cachoeiras de sinalização de proteínas quinases dependentes cíclicas, de maneira semelhante à AMP cíclica.
Foi descrito não apenas em mamíferos, que são animais de grande complexidade, mas também nos procariontes mais simples, incluídos nos reinos de eubactérias e arcos. Sua presença nas plantas ainda é uma razão para a discussão, mas as evidências sugerem que está ausente nesses organismos.
[TOC]
Treinamento e degradação
A concentração intracelular dos nucleotídeos cíclicos da guanina, bem como a da adenina, é extremamente baixa, especialmente se comparada à de seus análogos não cíclicos que são mono-, di- ou trifatizados.
No entanto, os níveis desse nucleotídeo podem ser seletivamente alterados na presença de certos estímulos hormonais e outros fatores que se comportam como mensageiros primários.
Pode servir a você: nucleoid: características, estrutura, composição, funçõesO metabolismo cíclico de GMP é parcialmente independente do metabolismo cíclico de AMP e outros nucleotídeos análogos. Isso é produzido a partir do GTP por um sistema enzimático conhecido como Guanilil Ciclassa ou Guanilaato Ciclasa, que é uma enzima parcialmente solúvel na maioria dos tecidos.
As enzimas da cilasase guanilato são responsáveis pela “ciclação” do grupo fosfato na posição 5 'do resíduo açucarado (ribose), causando a união do mesmo fosfato a dois grupos OH diferentes na mesma molécula.
Esta enzima é muito abundante nos pulmões do intestino delgado e dos mamíferos e a fonte mais ativa está no esperma de uma espécie de ouriço do mar. Em todos os organismos que foram estudados, depende de íons de manganês divalentes, que o diferenciam do adenilato de Cyclasas, que dependem de magnésio ou zinco.
A degradação cíclica de GMP é mediada por fosfodiesters de nucleotídeos cíclicos que não parecem ser específicos, pois foi demonstrado que as mesmas enzimas são capazes de usar, bem como substratos hidrolisíveis do AMP cíclico e cíclico GMP.
Ambos os processos, treinamento e degradação, são cuidadosamente controlados intracelularmente.
Estrutura
A estrutura do GMP cíclico não distribui consideravelmente a de outros nucleotídeos cíclicos. Como o nome indica (Guanosina 3 ', 5'-monofosfato) possui um grupo de fosfato ligado a oxigênio no carbono da posição 5' de um açúcar de ribose.
Esse açúcar ribose está ao mesmo tempo ligado à base de nitrogênio do anel heterocíclico de guanina por meio de uma ligação glicosídica com carbono na posição 1 'da ribose.
Pode atendê -lo: diossomoO grupo fosfato que é ligado ao átomo de oxigênio na posição de 5 'ribose é mesclado Trans Através de uma ligação fosfodiéster, que ocorre entre o mesmo grupo fosfato e o oxigênio do carbono na posição 3 'da ribose, formando um 3'-5'- “fosfatoTrans-fusado " (Do inglês 3'-5 '-Trans-fosfato fundido).
A fusão do grupo fosfato ou sua "ciclação" causa um aumento na rigidez da molécula, pois restringe a rotação livre dos elos no anel furano da ribose.
Como também é verdadeiro para o amplificador cíclico, a ligação glucosídica entre o anel de guanina e a ribose e sua liberdade de rotação são parâmetros estruturais importantes para o reconhecimento específico do GMP cíclico.
Funções
Ao contrário das funções múltiplas e variadas que outros nucleotídeos cíclicos análogos possuem, como AMP cíclico, a função GMP cíclica é um pouco mais restrita:
1 parte de participação nos processos de sinalização em resposta à estimulação da luz de pigmentos visuais. Sua concentração é modificada devido à ativação de uma proteína G que percebe o estímulo da luz e interage com uma fosfodiesterase de GMP cíclica dependente.
Alterações nos níveis deste alteração de nucleotídeos.
2-TI tem funções no ciclo de contração e relaxamento muscular do músculo liso em resposta ao óxido nítrico e a outros compostos químicos de natureza diversa.
Pode atendê -lo: diferenciação celular3-A O aumento de sua concentração devido à resposta contra peptídeos naturais está relacionado à regulação do movimento de íons de sódio e água através das membranas celulares.
4-em alguns organismos, o GMP cíclico pode competir com AMP cíclico por nucleotídeo cíclico fosfodiesterase.
5-Bactérias como E. coli Eles aumentam seus níveis cíclicos de GMP quando expostos a quimioatraientes, indicando que esse nucleotídeo está envolvido nos processos de sinalização em resposta a esses estímulos químicos.
6-foi determinado que o GMP cíclico também tem implicações importantes nos processos de vasodilatação e ereção em mamíferos.
Os canais de portão de iônios de 7 anos (cálcio e sódio) são regulados por ligantes intracelulares que usam especificamente o GMP cíclico.
Referências
- Botsford, j. eu. (1981). Nucleotídeos cíclicos em procariontes. Revisões microbiológicas, Quatro cinco(4), 620-642.
- Garrett, r., & Grisham, C. (2010). Bioquímica (4ª ed.). Boston, EUA: Brooks/Cole. Cengage Learning.
- Hardman, j., Robison, a., & Sutherland, e. (1971). Nucleotídeos cíclicos. Revisões anuais em fisiologia, 33, 311-336.
- Nelson, d. eu., & Cox, M. M. (2009). Lehninger Principles of Biochemistry. Edições Omega (5ª ed.).
- Newton, r. P., & Smith, C. J. (2004). Nucleotídeos cíclicos. Fitoquímica, 65, 2423-2437.

