Características da fucosa, estrutura, funções
- 5038
- 509
- Tim Mann
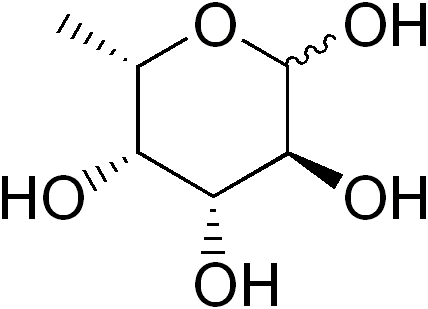
O Fucosa (FUC abreviado), ou 6-l-dexi-galactose, é um monossacarídeo parcialmente desoxigenado (deoxiazúcar) de seis carbonos cuja fórmula empírica é c é c é6H12QUALQUER5. Como outros monossacarídeos, é um açúcar poli -hidroxilado.
Quando um grupo hidroxila é substituído por um átomo de hidrogênio, um desoxiazúcar é derivado. Embora teoricamente essa substituição possa afetar qualquer grupo hidroxila de qualquer monossacarídeo, na natureza há pouca variedade de dexiazúcús.
 Fonte: Edgar181 [Domínio Público]
Fonte: Edgar181 [Domínio Público] Alguns desoxiazúces são: 1) Deoxyribosa (2-Disoxxi-D-Libose), derivado da Libose D, que faz parte do DNA; 2) o Ramnosa (6-D-Dexxi-Marso), derivado da D-mana; 3) Fucosa, derivada de L-galactose. O último é mais frequente que a D-fucosa, derivado de D-galactose.
[TOC]
Características e estrutura
Fucosa também é conhecida com nomes de 6-Disoxxi-Scalact-Hexose, Fucopiranous, Galactometil e Rodeous.
Embora normalmente esteja formando polissacarídeos e glicoproteínas, isolado como monossacarídeo é mais doce que a galactose. Isso ocorre porque a substituição de um grupo hidroxil por um átomo de hidrogênio aumenta o caráter hidrofóbico e, portanto, a doçura da molécula.
Os grupos hidroxila Fucosa podem experimentar as mesmas reações que outros açúcares, produzindo uma ampla variedade de acetais, glicosídeos, éteres e ésteres.
Uma biomolécula fucosilada é a que, pela ação de uma fucosiltransferase, eles se juntaram, por ligações glicosídicas, moléculas de fucosa. Quando a hidrólise das ligações glicosídicas ocorre pela ação de uma fucosidase, separando assim a fucosa, diz -se que a biomolécula foi defucosilada.
Quando os glucanos fucosil, glucanos mais complexos chamados fucanos são gerados, o que pode ou não fazer parte de glicoproteínas. Fucans em sulfato são definidos como os polissacarídeos que contêm resíduos de sulfato de L-fucosa. Eles são típicos de algas marrons. Como exemplos, eles podem ser nomeados Ascofilano, Sargasano e Pelvetano.
Um dos Fucanos mais bem estudados é o Fucoidano, obtido das algas marrons Fucus vesiculosus, que foi comercializado (Sigma-Aldrich Chemical Company) por décadas.
Pode atendê -lo: o que é o erristenoo?Distribuição na natureza
D-fucose está presente em substâncias antibióticas produzidas por micróbios e em glicosídeos vegetais, como complicação, charrtreusina, ledienosida e queirotoxina.
A L-fucose é um constituinte dos polissacarídeos das algas, os lençóis da ameixa, os revestimentos de linho, soja e canola, a borracha tragacanto, as paredes celulares da batata, os tubérculos da mandioca, a fruta kiwi, O córtex do CEIBA e o mucigel do miliptra de milho, bem como outras plantas.
L-Fucosa também está presente em ovos de ouriços do mar e na geléia que protege ovos de sapo.
Em mamíferos, os fucans com L-fucosa formam os ligantes que atuam na adesão leucócitos-endoteliais mediados por selectina e participam de numerosos eventos ontogenéticos.
A L-fucosa é abundante em fucoesphingolipids do epitélio gastrointestinal e medula óssea e aparece em pequenas proporções em cartilagem e estruturas queratinosas.
Em humanos, os fucanos com L-fucosa fazem parte de glicoproteínas de saliva e sucos gástricos. Eles também fazem parte dos antígenos que definem os grupos sanguíneos ABO. Eles estão presentes em vários oligossacarídeos de leite materno.
Metabolismo de Fucosa
Fucosiltransferases usam o PIB-fucose, uma forma de fucosa ativada por nucleotídeos, como doador de fucosa na construção de oligossacarídeos fucosilados.
A PIB-fucosa é derivada do PIB-mano para a ação sucessiva de duas enzimas: o GDP-ManaSea 4.6-desidratosa e o GDP-4-ZO-6-DESOXIMANOSA 3.5-EPIMERASA-4-REDUCTASE.
Uitlizando um cofator NADP+, a primeira enzima catalisa a desidratação do PIB-Many. A redução da posição 6 e a oxidação da posição 4 produz o PIB-6-desoxi-4-ceto-koaming (durante a reação, o híbrido é transferido da posição 4 para 6 do açúcar).
A segunda enzima, que depende do NADPH, catalisa a epimerização das posições 3 e 5, e a rede do grupo 4-zo, do PIB-6-desoxi-4-Ecto-mamosa.
As bactérias podem crescer usando Fucosa como uma única fonte de carbono e energia através de uma opeona induzível por fucosa que codifica enzimas catabólicas para este açúcar.
Pode atendê -lo: ácido carboxílicoO processo anterior envolve: 1) entrada gratuita da Fucosa através da parede celular com mediação de uma permeação; 2) isomerização da fucosa (um aldosa) para formar um fufuloso (um zea); 3) fosforilação do fuzuloso para formar fosfato fufuloso-1; 4) Uma reação da aldolase para formar fosfato de lacaldeído e di-hidroxiacetona a partir de fosfato de fucofuloso-1.
Funções
Papel de câncer
Entre os sintomas de muitos tipos de tumor carcinogênico estão a presença de proteínas ligadas a glucano que se distinguem por ter uma composição de oligossacarídeos alterados. A presença desses glucanos anormais, entre os quais Fucanos se destaca, está ligada à malignidade e ao potencial metastático desses tumores.
No câncer de mama, as células tumorais incorporam Fucosa em glicoproteínas e glicolipídios. Fucosa contribui para a progressão desse câncer, favorecendo a ativação de células -tronco cancerígenas, metástases hematogênicas e a invasão de tumores através de matrizes extracelulares.
No carcinoma pulmonar e hepatocarcinogênese, a expressão aumentada de fucosa está ligada ao alto potencial metastático e com baixa probabilidade de sobrevivência.
Como contraparte, alguns fucanos sulfatados são substâncias promissoras no tratamento do câncer, conforme determinado.
Papel em outras doenças
A expressão aumentada de Fucanos em imunoglobulinas séricas tem sido relacionada à artrite reumatóide juvenil e adulta.
A deficiência na adesão de leucócitos II é uma doença congênita rara devido a mutações que alteram a atividade de um transportador de FDP-luxuoso localizado no aparelho de Golgi.
Os pacientes sofrem de atraso mental e psicomotor e sofrem infecções bacterianas recorrentes. Esta doença responde favoravelmente às doses orais da fucosa.
Potencial biomédico
Sulfato Fucanos obtidos de algas marrons são reservatórios importantes de compostos com potencial terapêutico.
Pode atendê -lo: ititrium: estrutura, propriedades, usos, obtençãoEles têm propriedades anti -inflamatórias e antioxidantes, inibindo a migração de linfócitos em locais de infecção e favorecendo a liberação de citocinas. Aumente a resposta imune ativando linfócitos e macrófagos.
Eles têm propriedades anticoagulantes. Foi comprovado em pacientes humanos que inibem oralmente a agregação plaquetária.
Eles têm potencial antibiótico e antiparasitário e inibem o crescimento de bactérias patogênicas estomacais Helicobacter pylori. Mate parasitas Plasmodium spp. (Agente causal da malária) e Leishmania Donovani (Agente causal da leishmaniose americana visceotrópica).
Finalmente, eles têm poderosas propriedades antivirais, inibindo a entrada na célula de vários vírus de grande importância para a saúde humana, incluindo Arenavírus, Citomegalovírus, Hantavírus, Hepadnavirus, HIV, vírus herpes simplex e vírus influenza.
Referências
- Becker, d. J., Lowe, j. B. 2003. Fecose: biossíntese e função biológica em mamíferos. Glicobiologia, 13, 41R-53R.
- Deniaud-bouët, e., Hardouin, k., Potin, p., KLOAREG, b., Hervé, c. 2017. Uma revisão sobre paredes celulares de algas marrons e polissacarídeos sulfatados contendo fucose: contexto da parede celular, propriedades biomédicas e desafios de pesquisa-chave.Polímeros de carboidratos, http: // dx.doi.org/10.1016/j.Carbol.2017.07.082.
- Flores h. M. 1981. Química e bioquímica de D-e L-Fucose. Avanços na Química e Bioquímica de Carboidratos, 39, 279-345.
- Listinsky, J. J., Siegal, g. P., Listinsky, c. M. 2011. A importância emergente de α-L-luxuoso no câncer de mama humano: uma revisão. SOU. J. Trad. Carne bovina., 3, 292-322.
- Murray, r. K., et al. 2003. Bioquímica ilustrada de Harper. McGraw-Hill, Nova York.
- Pereira, l. 2018. Usos terapêuticos e nutricionais de algas. CRC Press, Boca Raton.
- Staudacher, e., Altmann, f., Wilson, i. B. H., März, l. 1999. Fucose em n-glicanos: de planta para homem. Biochimica et Biophysica Acta, 1473, 216-236.
- Tanner, w., Loewus, f. PARA. 1981. Carboidratos de plantas II. Carboidratos extracelulares. Springer, Nova York.
- Vanhooren, p. T., Vandamme, e. J. 1999. L-luxuoso: ocorrência, papel fisiológico, síntese química, enzimática e microbiana. Jornal de Tecnologia Química e Biotecnologia, 74, 479-497.
- « Localização do círculo polar antártico, características, flora e fauna
- Fases de quimiossíntese, organismos, diferenças com a fotossíntese »

