Estrutura cristalina
- 5049
- 1004
- Ralph Kohler
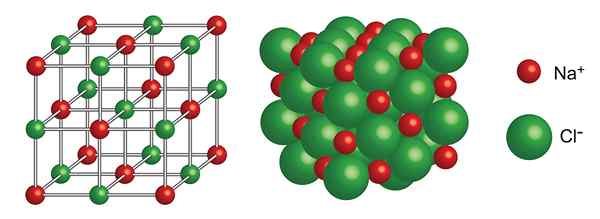
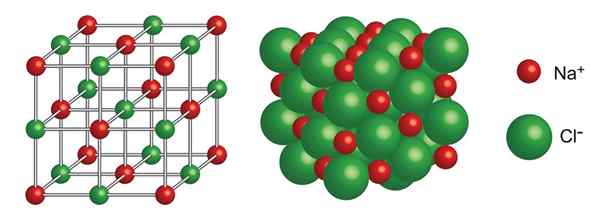 Estrutura cristalina de cloreto de sódio
Estrutura cristalina de cloreto de sódio Qual é a estrutura cristalina?
O estrutura cristalina Refere -se à maneira como átomos, íons ou moléculas são organizados ou embalados em sólidos cristalinos, como diamantes, sal (cloreto de sódio) ou açúcar (sacarose).
Sólidos cristalinos são formados em redes tridimensionais de unidades idênticas chamadas células unitárias. Estes se assemelham a pequenos blocos de construção idênticos (como layos) que se ligam para formar os cristais que podemos ver com a olho nu.
A estrutura cristalina consiste em uma descrição da forma desta célula unitária e a posição exata que cada átomo tem na referida célula.
Características da estrutura cristalina
São formados por células unitárias que são repetidas
A estrutura cristalina consiste na repetição de uma célula unitária em todas as direções. Essas células consistem em paralelepípedes tridimensionais cuja forma e tamanho são definidos por três vetores chamados a, b e c, e pelos ângulos entre esses vetores, chamados α, β e γ.
São estruturas altamente ordenadas
A estrutura cristalina é caracterizada por ser um dos estados mais ordenados que existem. Os cristais são ordenados que, ao conhecer a estrutura da célula unitária que contém apenas um punhado de átomos, toda a estrutura de um vidro formado por milhões de átomos, íons ou moléculas possa ser reconstruído.
Eles apresentam simetria
A maioria das células unitárias com as quais sólidos cristalinos podem ser construídos têm algum tipo de simetria. Isso significa que o conteúdo de uma parte da célula é repetido em outra parte dela depois de realizar uma rotação, reflexão ou investimento.
Pode servir a você: Secador rotativo: operação, para que serve, peças, aplicaçõesPor exemplo, se uma célula unitária tem um plano de simetria, isso significa que metade da célula é o reflexo do outro.
Relação entre propriedades da matéria e estrutura cristalina
Existem muitas propriedades físicas e químicas que dependem da estrutura cristalina:
Densidade
Dependendo da maneira como os átomos são embalados na estrutura cristalina, estruturas ou estruturas mais compactas podem ser obtidas nas quais os átomos estão mais longe um do outro. No primeiro caso, será obtido um sólido denso e pesado, pois mais átomos são embalados em um volume mais baixo.
-
Exemplo
Se compararmos as três estruturas cristalinas cúbicas chamadas simples cúbicas (P), centradas cúbicas em faces (FCC) e cúbico centrado no corpo (BCC) para átomos iguais, a estrutura do BCC é 2 é 2.6 vezes mais denso que a FCC, e a FCC é 1.4 vezes mais denso que P.
Forma cristalina
A forma dos cristais que podemos ver a olho nu é um reflexo da estrutura cristalina e, em particular, da célula unitária. Dependendo da estrutura da célula unitária, os cristais crescerão mais em uma direção do que em outros, o que dá origem a cristais com diferentes formas, como agulhas, cotas, cristais hexagonais, etc.
Anisotropia
Propriedades físicas, como condutividade térmica ou elétrica e as propriedades magnéticas da matéria, geralmente são maiores em uma direção material do que em outro.
Isso é chamado de anisotropia, e esses efeitos são particularmente intensos em estruturas cristalinas porque são estruturas muito ordenadas e regulares.
Pode atendê -lo: DIRETEOMERSTipos de estrutura cristalina
Estruturas cristalinas podem ser classificadas de acordo com o tipo de célula unitária pela qual são formadas. Estes são caracterizados pelos três lados que se conectam a uma de suas bordas (chamada A, B e C) e pelos ângulos entre esses lados (chamados α, β e γ).
Isso dá origem a 7 sistemas cristalinos. Dentro de cada um desses sistemas cristalinos, diferentes tipos de células unitárias podem ser distinguidos. No total, existem 14 células unitárias diferentes que são chamadas de 14 redes Bravais e estão representadas abaixo:
Sistema cúbico
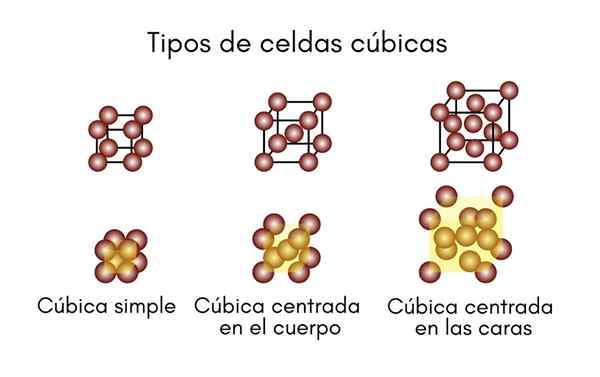
Como o nome indica, a célula unitária consiste em um cubo perfeito. Os três lados, A, B e C são iguais um ao outro, e seus três ângulos são todos 90 °. Este sistema consiste em células:
- Simples ou primitivo cúbico.
- Cúbico centrado no corpo (BCC).
- Cúbico centrado em rostos (FCC).
Sistema tetragonal
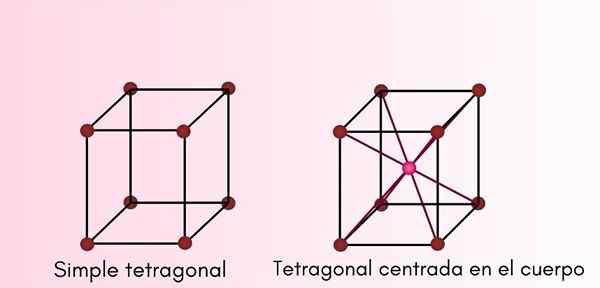
Nesse tipo de estrutura cristalina, A e B são os mesmos, mas C é diferente, mas todos permanecem perpendiculares um ao outro. As células tetragonais podem ser:
- Tetragonal simples ou primitivo.
- Tetragonal centrado no corpo.
Sistema Ortorrombic
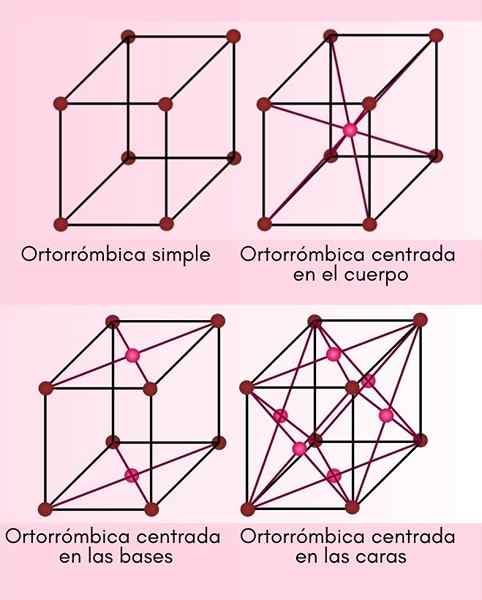
Neste sistema cristalino, A, B e C são todos diferentes, mas ainda são perpendiculares um ao outro. Existem 4 células Ortorrombic diferentes:
- Primitivo ou simples ortorrômbico.
- Orthrome central do corpo.
- Orthrome centrada na base.
- Ortorombic centrado na face.
Sistema monoclínico
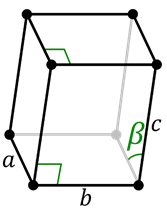 Célula monoclínica primitiva
Célula monoclínica primitiva 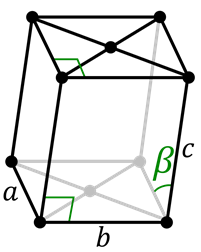 Célula monoclínica centrada na base
Célula monoclínica centrada na base O sistema monoclínico é semelhante ao hexagonal, exceto pelo fato de que todos os seus lados são diferentes. Existem duas células para o sistema monoclínico:
- Monoclínico primitivo.
- Monoclínico centrado na base.
Sistema triclínico
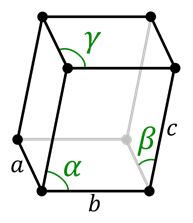 Célula triclínica
Célula triclínica No sistema de triciciclismo, não há simetria. Todos os ângulos são diferentes um do outro e não necessariamente precisam ser 90 °. Todos os seus lados também são diferentes.
Sistema hexagonal
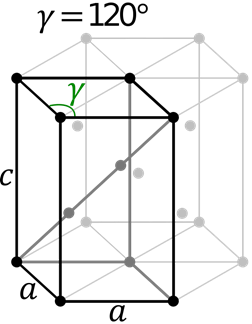 Célula hexagonal
Célula hexagonal Esta célula contém os lados A e B diferentes e diferentes do lado C. Os ângulos α e β são 90 °, enquanto γ = 120 °.
Sistema trigonal ou romboyan
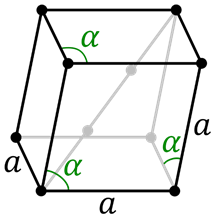 Célula trigonal ou romboedical
Célula trigonal ou romboedical Este é um tipo particular de estrutura semelhante a pegar um balde e esticá -lo ao longo de dois vértices opostos. Todos os lados são iguais e também seus ângulos, mas estes não são 90 °.
Exemplos de estruturas cristalinas
Cloreto de sódio
Sua estrutura cristalina consiste em uma rede cúbica centrada em faces com 4 unidades de NaCl para cada célula unitária,
Alfa Ferro
Ferro cristaliza o ferro alfa a 768 ° C. Sua estrutura é cúbica centrada no corpo com uma 2ª borda de 2.86 Å (ou 286 pm)
Ferro gama
É uma forma de ferro que ocorre entre 910 ° C e 1400 ° C e possui uma estrutura cristalina cúbica centrada nas faces de 3.64 Å (364 pm) da borda.
Diamante
O diamante é uma das formas de carbono mais valiosas e possui uma estrutura cristalina cúbica centrada em faces (FCC) que contém dois átomos de carbono e uma borda de 3 de 3.75 Å (375 pm).
Grafite
Grafite é outro carbono muito comum. Nesse caso, essas são folhas de átomos de carbono juntos, formando anéis de 6 membros, que dão origem a uma estrutura cristalina hexagonal.

