Alkynes
- 3377
- 477
- Gilbert Franecki
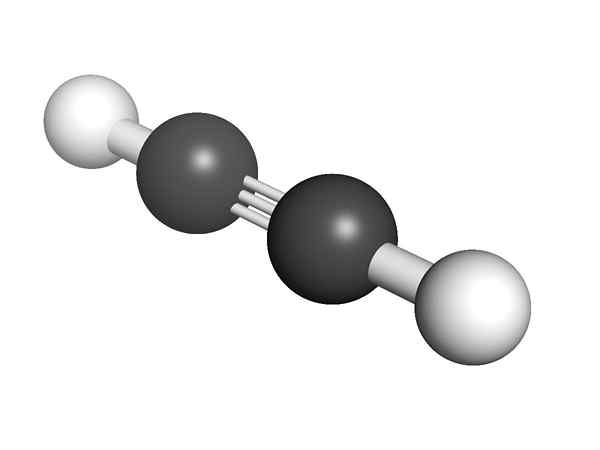
 Estrutura alvento, com um link triplo
Estrutura alvento, com um link triplo O que são Alcines?
O Alkynes São hidrocarbonetos ou compostos orgânicos que apresentam em suas estruturas um vínculo triplo entre dois carbonos. Este link triplo (≡) é considerado um grupo funcional ao representar um local ativo da molécula e, portanto, é responsável por sua reatividade.
Embora as alcinos não se diferenciem muito de Alko ou Alkenes, eles exibem maior acidez e polaridade devido à natureza de seus links. O termo preciso para descrever essa pequena diferença é o que é conhecido como insaturação.
Os alcanos são hidrocarbonetos saturados, enquanto os alcinos são os mais insaturados em relação à estrutura original. O que significa isto? Que um alcano h3C-CH3 (etano) pode ser desidrógeno para h2C = ch2 (etene) e subsequentemente HCidor (Etino, ou mais conhecido como acetileno).
Observe como os links adicionais são formados entre os carbonos diminui o número de hidrogênios vinculados a eles. O carbono, devido às suas características eletrônicas, procura formar quatro links simples, de modo que maior a tendência a reagir (exceto por compostos aromáticos).
Por outro lado, o link triplo é muito mais forte que o duplo (=) ou a ligação simples (-), mas a um alto custo de energia. Portanto, a maioria dos hidrocarbonetos (alcães e alcenos) pode formar ligações triplas a altas temperaturas.
Como conseqüência das altas energias destes, ao quebrar, elas liberam muito quentes. Um exemplo desse fenômeno pode ser visto quando o acetileno queima com oxigênio e o calor intenso da chama para soldar ou derreter metais é usado.
Acetileno é o alcino mais simples e pequeno de todos. Outros hidrocarbonetos podem ser expressos a partir de sua fórmula química, substituindo H por grupos alquilicais (RCidor '). O mesmo acontece no mundo da síntese orgânica através de um grande número de reações.
Este alcino ocorre a partir da reação do óxido de cálcio do calcário e do coque, matéria -prima que fornece os carbonos necessários dentro de um forno elétrico:
Cao + 3c => CAC2 + Co
O CAC2 É o carboneto de cálcio, um composto inorgânico que finalmente reage com a água para formar acetileno:
CAC2 + 2h2O => CA (OH)2 + HCidor
Propriedades físicas e químicas de Alcines
Polaridade
O link triplo distingue alcinos de alcans e alcenos. Os três tipos de hidrocarbonetos são apolares, insolúveis em água e ácidos muito fracos. No entanto, a eletronegatividade dos carbonos de ligação dupla e tripla é maior que a dos carbonos simples.
De acordo com isso, carbonos adjacentes ao rendimento triplo de ligação ao efeito indutivo densidade de carga negativa. Por esse motivo, onde estão os links C≡C ou C = C, haverá maior densidade eletrônica do que no restante do esqueleto carbonatado. Como conseqüência, há um pequeno momento de dipolo em que as moléculas interagem por forças dipolo-dipolo.
Essas interações são muito fracas se seus momentos dipolares forem comparados com os da molécula de água ou qualquer álcool. Isso se reflete em suas propriedades físicas: os alcinos geralmente têm maiores pontos de fusão e ebulição em comparação com os de seus hidrocarbonetos menos insaturados.
Pode atendê -lo: os 7 aplicativos de bioquímica mais importantesDa mesma forma, devido à sua baixa polaridade, eles são menos insolúveis em água, mas solúveis em solventes orgânicos apolares, como o benzeno.
Acidez
Além disso, essa eletronegatividade causa hidrogênio HCIador é mais ácido do que qualquer um presente em outros hidrocarbonetos. Portanto, os alcinos são espécies mais ácidos que os alcenos e muito mais que os alcaneos. No entanto, sua acidez permanece desprezível se comparada à dos ácidos carboxílicos.
Como os álcines são ácidos muito fracos, eles apenas reagem com bases muito fortes, como o sódio Amiduro:
HC teve NANH2 => Hc 3.CNA + NH3
A partir desta reação, é obtida uma solução de acetilura de sódio, matéria -prima para a síntese de outros alcinos.
Reatividade de Alquinos
A reatividade dos alcinos é explicada pela adição de pequenas moléculas ao seu link triplo, diminuindo sua insaturação. Estas podem ser moléculas de hidrogênio, hidrogenídeos de hidrogênio, água ou halogênios.
Hidrogenação
A pequena molécula H2 É muito esquivo e rápido, por assim dizer, aumentar as chances de ser adicionado ao link triplo dos Alcines.
Geralmente, são metais (Pd, Pt, Rh ou Ni) divididos finamente para aumentar a área da superfície; E dessa maneira, o contato entre o hidrogênio e o Alquino:
Rc tal ' + 2h2 => Rch2CH2R '
O resultado é que o hidrogênio é "âncora" para carbonos quebrando um vínculo, e assim por diante até que o Alkane correspondente produza, RCH2CH2R '. Isso não apenas satura o hidrocarboneto inicial, mas também modifica sua estrutura molecular.
Adição de hidrogênio halogenuros
Aqui é adicionada a molécula inorgânica HX, onde x pode ser qualquer um dos halogênios (F, Cl, Br ou I):
Rc tal ' + hx => rch = cxr'
Hidratação
A hidratação de Alcines é quando eles adicionam uma molécula de água para formar um aldeído ou uma cetona:
Rc tal ' + h2O => rch2Cor '
Se r 'é um H, é um aldeído; Se for um aluguel, então é um Cetona. Na reação, um composto conhecido como enol (rch = c (oh) r ') é formado como intermediário.
Isso sofre uma conversão da forma enólica (C-OH) em cetona (C = O) em um equilíbrio chamado tautomerização.
Adição de halogênios
E com relação às adições, as moléculas diatômicas de halogênios também podem ser ancoradas em carbonos (x x2= F2, Cl2, Br2 ouvi2):
Rc tal ' + 2x2 => Rcx2-Cx2R '
Alquilação de acetileno
A partir da solução de acetilura de sódio, outros alcinos podem ser preparados usando um halogeneto de aluguel:
HCidor
Por exemplo, se fosse o iodeto de metila, então o alcino resultante seria:
HC teve CH3I => hc 3.CCH3 + Nax
HCidor3 é o apropriado, também conhecido como Metiloacetileno.
Estrutura química de Alcines
 Estrutura química do Alquino
Estrutura química do Alquino Qual é a estrutura dos alcinos? Na imagem superior, uma molécula de acetileno é mostrada. A geometria linear do link C≡C pode ficar claro a partir dele.
Portanto, onde há uma ligação tripla, a estrutura da molécula deve ser linear. Essa é outra das diferenças notáveis entre eles e o resto dos hidrocarbonetos.
Pode atendê -lo: Cycopropano (C3H6)Os alcaneos geralmente são representados como ziguezague, porque têm hibridação de SP3 e seus links estão separados de 109º. Eles são na verdade uma cadeia de tetraedra covalentemente unida. Enquanto os alcenos são planos por hibridação SP2 de seus carbonos, formando mais especificamente um plano trigonal com links separados por 120º.
Em alcinos, a hibridação orbital é SP, ou seja, eles têm 50% de A se 50% de um P. Existem dois orbitais híbridos SP que estão ligados a átomos H em grupos acetileno ou alcino nos alcinos.
A distância H ou R é 180º, além do fato de que somente dessa maneira os carbonos puros orbitais podem formar o título triplo. Por esse motivo, o link -c tal é linear. Vendo a estrutura de qualquer molécula os destaques -c marc nas regiões onde o esqueleto é muito linear.
Distância dos links e esmolas terminais
Os carbonos na ligação tripla estão a uma distância menor do que no link duplo ou simples. Em outras palavras, Cñc é mais curto que C = C e que C-C. Como resultado, o link é mais forte porque os dois links π contribuem para estabilizar o link simples σ.
Se a ligação tripla estiver no final de uma corrente, então é um alcino terminal. Portanto, a fórmula do referido composto deve ser HCidor, onde o H observa o fim ou o início da cadeia.
Se, pelo contrário, é um link interno triplo, a fórmula é rc tal ', onde r e r' são o lado direito e esquerdo da corrente.
Nomenclatura dos Alquinos
Como os Alcines são nomeados de acordo com as regras ditadas pelo IUPAC? Da mesma maneira que os alquenos e alcenos foram nomeados. Para fazer isso, o sufixo -ano ou -Eno para o sufixo -ino é alterado.
Por exemplo: HCidor3 É nomeado dicas, pois possui três carbonos, como o propano (CHO3CH2CH3). O HCidor2CH3 É o 1-Butino, que é um alcino terminal. Mas no caso de Cho3Ctalcch3 Este é o 2-butino e, neste link triplo, não é terminal, mas interno.
O ch3Ctalcch2CH2(CH3)2 É 5-metil-2-hexina. Os carbonos começam do lado mais próximo do link triplo.
Outro tipo de alcines são os cicloalquins. Para eles, basta substituir o sufixo -ano por -ino do cicloalcan correspondente. Assim, o ciclopropano que possui uma ligação tripla é nomeado como ciclopropina (que não existe).
Quando há dois links triplos, o prefixo di é adicionado ao nome-. Tem como exemplos para HCidor-C marcidor, diacetileno ou propadina; E para HCidor.
Alquinos usa
Acetileno ou etino
O menor dos alcinos engrossa o possível número de usos para esses hidrocarbonetos. A partir dele através de Alks, outros compostos orgânicos podem ser sintetizados. Também sofre reações oxidativas para obter etanol, ácido acético, ácido acrílico, entre outros.
Pode atendê -lo: hidreto de lítio: estrutura, propriedades, obtenção, usosOutros de seus usos consistem em fornecer a fonte de calor para excitar os elétrons dos átomos; Mais específico, e de cátions metálicos em determinações por emissão de absorção atômica, técnica espectroscópica amplamente usada.
Alcines naturais
Os únicos métodos existentes para preparar alcinos não são apenas sintéticos ou com aplicação de calor na ausência de oxigênio, mas também biológica.
Nessas enzimas chamadas acetilês, que pode negar um vínculo duplo. Graças a isso, muitas fontes naturais de alcinos são alcançadas.
Depois disso, essas fontes podem ser venenos extraídos, antídotos, medicamentos ou qualquer outro composto que ofereça qualquer benefício; Especialmente quando se refere à saúde. As alternativas são muitas ao modificar suas estruturas originais e tê -las como suporte para novos Alcines.
Exemplos de alcinos
Até agora, numerosos exemplos de alcinas foram mencionados. No entanto, alguns vêm de fontes muito específicas ou têm estruturas moleculares específicas: elas são poliacicyle.
Isso significa que pode haver mais do que um link triplo que faz parte de uma estrutura muito grande, e não apenas de uma corrente carbonatada simples.
Ácido taríico
 Estrutura do ácido tálico
Estrutura do ácido tálico O ácido taríico vem de uma planta localizada na Guatemala chamada Picramnia Tariri. É especificamente extraído do óleo de suas sementes.
Em sua estrutura molecular, pode -se observar um único link triplo que separa uma cauda apolar de uma cabeça polar; Portanto, pode ser considerado como uma molécula anfipática.
Histriototoxina
 Estrutura de histriionicotoxina
Estrutura de histriionicotoxina Histriototoxina é um veneno segregado pela pele dos habitantes da Colômbia, Brasil e outros países da América Latina. Possui dois links conjugados triplos com um vínculo duplo. Ambos são terminais e são separados por um anel de seis carbonos e uma amina cíclica.
Cicutoxina
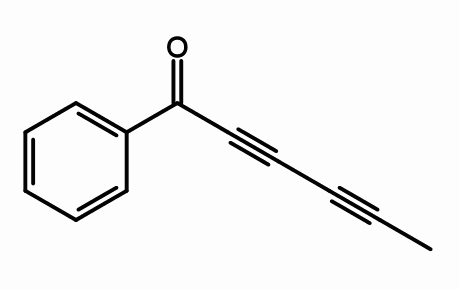 Estrutura da cicutoxina. Por giorgiogp2 [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0) ou GFDL (http: // www.gnu.Org/copyleft/fdl.html)], da Wikimedia Commons
Estrutura da cicutoxina. Por giorgiogp2 [CC BY-SA 3.0 (https: // CreativeCommons.Org/licenças/BY-SA/3.0) ou GFDL (http: // www.gnu.Org/copyleft/fdl.html)], da Wikimedia Commons Da estrutura molecular da cicutoxina, onde estão os links triplos? Se as ligações duplas forem planas, como são vistas corretas e os links simples são tetraedros, pois nas extremidades, os triplos são lineares e estão na inclinação (\).
Este composto consiste em uma neurotoxina encontrada principalmente na planta de cura aquática.
Capillina
 Estrutura de capillina. Por Klever [CC0], da Wikimedia Commons
Estrutura de capillina. Por Klever [CC0], da Wikimedia Commons É um alcino presente no óleo essencial de plantas artemis que é usado como um agente antifúngico. Dois links consecutivos triplos podem ser observados, mais corretamente conjugados.
Que significa? Que as ligações triplas ressoam ao longo de toda a cadeia de carbono e envolve que a ligação dupla C = O é aberta para C-O-.
Pargilina
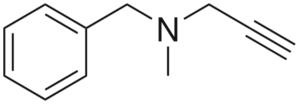 Estrutura de pargilina
Estrutura de pargilina É um ALTY com atividade anti -hipertensiva. Analisando sua estrutura em partes é: um grupo Benchilo à esquerda, uma amina terciária no meio e uma permanência direita; isto é, um grupo de propriedades terminais.
Referências
- Francis a. Tortoisshell. Quimica Organica. Ácidos carboxílicos. (Sexta edição., Página 368-397). Mc Graw Hill.
- Brennan, John. (10 de março de 2018). Exemplo de alcinos. Cienting. Retirado de: Cienting.com
- Byju's. (2018). Vínculo triplo em alcinos. Retirado de: Byjus.com
- Enciclopédia de exemplos (2017). Alkynes. Recuperado de: exemplos.co
- Kevin a. Boudreaux. Alkynes. Retirado de: Angelo.Edu
- Robert c. Neuman, jr. Alcenos e Alcinos. [PDF]. Tirado de: química.Ucr.Edu

