Conceito de agente oxidante, os exemplos mais fortes
- 1597
- 154
- Shawn Leffler
A agente oxidante É um produto químico que tem a capacidade de subtrair elétrons de outra substância (agente redutor) que doa ou perde. Também é conhecido como um agente oxidante nesse elemento ou composto que atravessa átomos eletronegativos para outra substância.
Quando as reações químicas são estudadas, todas as substâncias envolvidas e os processos que ocorrem neles devem ser levados em consideração. Entre os mais importantes estão as reações de redução de óxido, também chamadas redox, que envolvem a transferência ou transferência de elétrons entre duas ou mais espécies químicas.

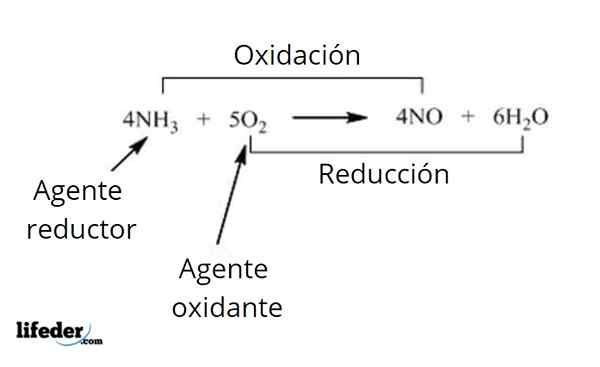
Nessas reações, duas substâncias interagem: o agente redutor e o agente oxidante. Alguns dos agentes oxidantes que podem ser observados com mais frequência são oxigênio, hidrogênio, ozônio, nitrato de potássio, perborato de sódio, peróxidos, halogênios e compostos de permanganato, entre outros.
O oxigênio é considerado o mais comum de agentes oxidantes. Como exemplo dessas reações orgânicas que envolvem a transferência de átomos, a combustão se destaca, que consiste em uma reação produzida entre oxigênio e algum outro material oxidável.
[TOC]
O que são agentes oxidantes?
Na semi -retirada de oxidação, o agente oxidante é reduzido porque, ao receber elétrons do agente redutor, uma diminuição no valor da carga ou número de oxidação de um dos átomos do agente oxidante é induzido.
Isso pode ser explicado pela seguinte equação:
2mg (s) + o2(g) → 2MGO (s)
Pode -se observar que o magnésio (Mg) reage com oxigênio (O2) e que o oxigênio é o agente oxidante porque subtrai os elétrons do magnésio - ou seja, está sendo reduzido - e o magnésio se torna, por sua vez, no seu Agente de reação da reação.
Pode atendê -lo: calcógenos ou anfumosDa mesma forma, a reação entre um forte agente oxidante e um forte agente redutor pode ser muito perigoso, porque eles podem interagir violentamente, para que sejam armazenados em sites separados.
Quais fatores definem a força de um agente oxidante?
Essas espécies são distinguidas de acordo com sua "força". Ou seja, o mais fraco são aqueles que têm uma capacidade menor de subtrair elétrons de outras substâncias,.
Em vez disso, os mais fortes têm maior facilidade ou capacidade de "iniciar" esses elétrons. Para sua diferenciação, as seguintes propriedades são consideradas:
Rádio atômico
É conhecido como metade da distância que separa os núcleos de dois átomos de elementos metálicos adjacentes ou "vizinhos".
Os rádios atômicos são geralmente determinados pela força com a qual os elétrons mais superficiais são atraídos para o núcleo do átomo.
Portanto, o raio atômico de um elemento diminui na tabela periódica de baixo para cima e da esquerda para a direita. Isso implica que, por exemplo, o lítio tem um raio atômico significativamente maior que o fluoreto.
Eletro-negatividade
A eletronegatividade é definida como a capacidade de um átomo de capturar elétrons pertencentes a uma ligação química a si mesma. À medida que a eletronegatividade aumenta, os elementos têm uma tendência crescente de atrair elétrons.
Em termos gerais, a eletronegatividade aumenta da esquerda para a direita na tabela periódica e diminui enquanto o caráter metálico cresce, sendo o fluorino o elemento mais eletronegativo.
Afinidade eletrônica
Dizem que é a variação da energia registrada quando um átomo recebe um elétron para gerar um ânion; Isto é, é a capacidade de uma substância receber um ou mais elétrons.
Pode servir a você: Substituição eletrofílica aromática: mecanismo e exemplosÀ medida que a afinidade eletrônica aumenta, a capacidade oxidativa de uma espécie química aumenta.
Energia de ionização
É a quantidade mínima de energia necessária para iniciar um elétron de um átomo ou, em outras palavras, é uma medida da "força" com a qual um elétron está ligado a um átomo.
Quanto maior o valor dessa energia, o desapego de um elétron é mais difícil. Assim, a energia de ionização é aumentada da esquerda da direita e é reduzida de cima para baixo na tabela periódica. Nesse caso, os gases nobres têm grandes valores de energia de ionização.
Os agentes oxidantes mais fortes
Levando em consideração esses parâmetros dos elementos químicos, é possível determinar quais são as características que os melhores agentes oxidantes devem ter: alta eletronegatividade, em rádio atômico e alta energia de ionização.
Dito isto, os melhores agentes oxidantes são considerados capazes de oxidar um grande número de substâncias.
Exemplos de reações com agentes oxidantes
Em algumas reações de redução de óxido, é mais fácil visualizar a transferência de elétrons do que nos outros. Alguns dos exemplos mais representativos serão explicados abaixo:
Exemplo 1
A reação de decomposição do óxido de mercúrio:
2HGO (S) → 2HG (L) + O2(g)
Nesta reação, o mercúrio (agente oxidante) é distinguido como o receptor de elétrons de oxigênio (agente redutor), decompondo em mercúrio líquido e oxigênio a gás ao aquecer.
Pode servir a você: ácido láúrico: estrutura, propriedades, usos, benefícios, efeitosExemplo 2
Outra reação que exemplifica a oxidação é a queima de enxofre na presença de oxigênio para formar dióxido de enxofre:
S (s) + O2(g) → Então2(g)
Aqui pode -se observar que a molécula de oxigênio é oxidada (agente redutor), enquanto o enxofre elementar é reduzido (agente oxidante).
Exemplo 3
Finalmente, a reação de combustão de propano (usada no gás para aquecimento e cozinha):
C3H8(g) + 5o2(g) → 3CO2(g) + 2h2Ou (l)
Nesta fórmula, a redução de oxigênio (agente oxidante) pode ser observada.
Referências
- Agente redutor. Recuperado de.Wikipedia.org
- Chang, R. (2007). Química, nona edição (McGraw-Hill).
- Malone, l. J., E Dolter, T. (2008). Conceitos básicos de química. Recuperado de livros.Google.co.ir
- Ebbing, d., E Gammon, S. D. (2010). Química Geral, edição aprimorada. Recuperado de livros.Google.co.ir
- Kotz, J., Treichel, p., E Towsend, J. (2009). Química e reatividade química, edição aprimorada. Recuperado de livros.Google.co.ir
- « Características da montanha alta, clima, fauna, flora, localização
- Características da arte mesopotâmica, pintura, escultura, cerâmica »

